大学で化学を学ぶとき、多くの人で理解できないものにσ結合(シグマ結合)とπ結合(パイ結合)があります。この2つの結合の意味を理解できないため、教授が講義で何を言っているのか分からないのです。
しかし本来、σ結合とπ結合の考え方は非常に簡単です。物質同士が結合するとき、しっかりくっついているのか、ゆるく結合しているのかの違いだけです。この概念さえ学べば、σ結合とπ結合を完ぺきに理解できるようになります。
またσ結合とπ結合を理解することで、化学物質の反応性を理解できるようになります。また、共有結合での二重結合、三重結合の反応性も理解できます。
ここでは、σ結合 π結合の違いや性質・特徴を分かりやすく解説していきます。
もくじ
高校化学の二重結合のイメージを忘れるべき
化合物の二重結合を理解するとき、どのようなイメージをもっているでしょうか。分子の模型を組み立てるときを含め、高校化学を習った人では、以下のような結合のイメージを有している人が大多数です。
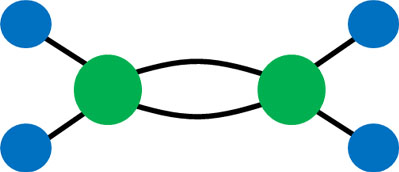
ただ、この分子イメージは忘れてください。このイメージがあなたの頭にある限り、化学でのσ結合やπ結合を理解することはできません。
分子が結合しているとき、こうした単純な形ではなく、実際には特殊な形によって結合しています。分子同士の結合には種類があり、それがσ結合とπ結合というわけです。σ結合とπ結合は明確に区別しなければいけません。
SP3混成軌道はs軌道・p軌道で4つの手が存在する
原子が結合するとき、自分の手を出す必要があります。原子の手とは、電子軌道のことを指します。
それぞれの原子または分子には軌道があります。これらの軌道をs軌道やp軌道といいます。単結合の炭素原子に着目すると、炭素原子は1つのs軌道と3つのp軌道が加わることで、4つの手が存在することになります。つまり、炭素原子は4ヵ所で結合することができます。
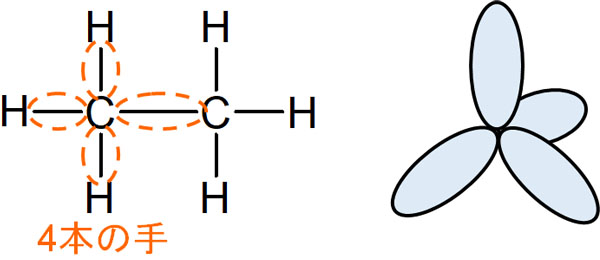
このようにエタンであれば、一つの炭素原子が4つの原子と結合しています。炭素原子で4本の手が存在するのは理解できるはずです。s軌道やp軌道によって4つの手が存在する場合、これをsp3混成軌道といいます。
sp3混成軌道の場合、いろんな方向に手が出ています。特定の方向だけ手を出せるわけではなく、4つの手はバラバラの方向を向いているのです。
電子はマイナスの電荷を帯びています。そのため、それぞれの手は互いに反発しており、結果としてそれぞれの手は異なる方向に向いています。
ただ、s軌道やp軌道、sp3混成軌道などの言葉が出てくると非常に内容が複雑になります。そこで最初、炭素原子は4つの手が存在し、他の原子や分子と結合できることだけ理解しましょう。
σ結合(シグマ結合)は共有結合を形成し、結合エネルギーは高い
炭素原子は4つの手を利用して、他の原子や分子と結合できます。それでは、炭素原子が他の原子や分子と単結合(一ヵ所での結合)する場合、どのように結合するでしょうか。当然、最も簡単な方法を選択します。自分の手を相手に出し、単結合します。
これがσ結合(シグマ結合)です。
人間でいうと、相手と握手をするとき、特に不自由することなく片腕を差し出して握手することができます。相手と強い力で手を握ることができ、これがσ結合のイメージです。
強く握手できるため、簡単に結合が切れて離れることはありません。σ結合は非常に結合エネルギーが高く、結合力は強いです。電子軌道同士が重なることで、結合を作ります。
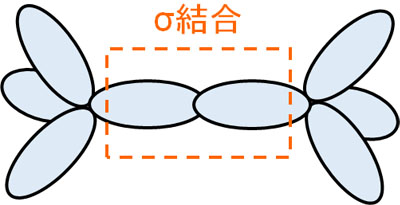
当たり前のことを言っているように思いますが、この事実を理解しないと、π結合を理解することはできません。
いずれにしても、無理な体勢を取ることなく、相手と手をつなげる状態がσ結合です。共有結合の中でもσ結合は非常に結合エネルギーが強く、状態は安定しています。これは、自分の手を伸ばして相手と強く結合できるからです。
単結合のσ結合は回転することが可能:エタンの例
またσ結合(シグマ結合)だけで分子を構成している場合、単結合になります。C-CやC-Hの結合は単結合であり、一本の手だけでつながっています。
単結合の場合、σ結合は回転することができます。例えばエタンの場合、すべて単結合であり、どれもσ結合です。そのためエタンでは、すべての結合で自由に軸を回転させることができます。以下はエタンの構造式です。

炭素原子がほかの原子や分子と結合する場合、最初は必ずσ結合します。単結合はどれもσ結合であり、非常に強い結合です。
エタンは反応性が低いことで知られています。有機化合物が反応して他の化合物が生成されるためには、結合が切れなければいけません。ただσ結合は結合エネルギーが強く、分子同士が強く結びついているため、有機化合物同士で反応を起こすのは難しくなっています。
有機化学反応でエタンに非常に強いエネルギーを加えないと反応しないのは、エタンがすべて単結合(σ結合)で構成されているからです。
π結合(パイ結合)は結合軸に対してゆるく結合する
一方、共有結合にはσ結合だけでなく、π結合(パイ結合)も存在します。同じ共有結合であっても、種類があります。σ結合とπ結合は別に考えなければいけません。
先ほどまで、単結合について解説してきました。「単結合=σ結合」と認識すればいいです。一方、有機化合物の中には二重結合や三重結合を有する化合物が存在します。単結合ではなく、二重結合や三重結合をもつ化合物では、π結合ももつようになります。
「二重結合や三重結合=π結合がある」と理解しましょう。
それでは、π結合とは何なのでしょうか。先ほど、相手に対して手を差し出して握手をするのがσ結合だと説明しました。一方でπ結合では、相手に向かって手を差し出すのではなく、手を真上に伸ばすようにしましょう。この状態で何とかして相手と握手します。

手を上に伸ばした状態で握手をするのは、非常に難しいように思えてしまいます。しかも相手と距離がある状態だと、手をつなぐのは不可能です。いずれにしても、真上に手を伸ばして手をつなぐのは困難だと分かります。
炭素原子が他の分子と結合し、手をつなぐとき、前述の通り最初は必ずσ結合となります。ただ単結合ではなく、二重結合を作る場合はどうすればいいのでしょうか。
sp3混成軌道で説明した通り、炭素から出ている4本の手は方向がバラバラです。人間のように腕を自由に動かせるわけではなく、手を伸ばせる向きは既に決められています。腕の位置が固定されているわけです。
二重結合・三重結合はπ結合が関わる
二重結合を作る場合、この状態で何とかして手を伸ばし、相手の原子と握手しなければいけません。つまり自分の腕を真上に伸ばした状態にて、何とかして結合する必要があります。その結果、電子たちは以下のように結合します。
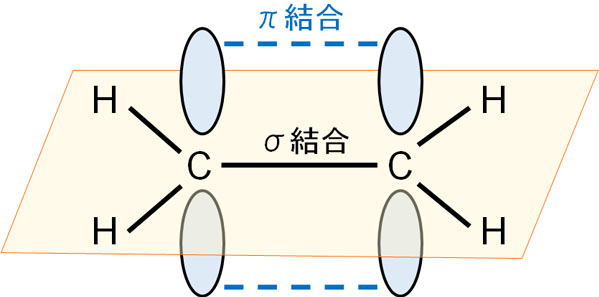
結合軸に対して垂直に手を出した後、頑張って結合する状態がπ結合です。σ結合のように相手に向かって手を出せない理由としては、既に述べた通り、人間のように自由に腕を動かせないからです。腕の場所は固定されています。
悪い体勢で手を握るため、σ結合に比べると、π結合は弱いです。つまり結合エネルギーが低く、強く手を握ることはできません。二重結合では、一つのσ結合と一つのπ結合が存在します。
一方、三重結合ではどうなのでしょうか。三重結合では、同じようにσ結合だけでなく、π結合によって原子同士が結合します。
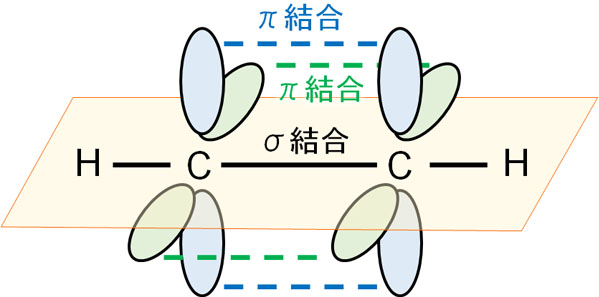
σ結合の結合軸に対して、横に手を伸ばすのは同じです。この状態から頑張って手を伸ばし、手を握ろうとします。三重結合では、一つのσ結合と二つのπ結合となります。
σ結合では、電子軌道が重なることで結合を作ります。一方、π結合は電子軌道が重なるというより、電子雲(電子が雲のように存在する状態)が薄く重なった状態をイメージすればいいです。
反応性が高い二重結合・三重結合のπ結合:エチレン、アセチレンの例
分子同士が強く結合しており、結合エネルギーが強いのがσ結合です。一方でπ結合(パイ結合)は強く結合しておらず、手を握る力は弱いです。そのため、有機合成での反応性が高くなっています。
有機化合物同士が反応を起こすとき、以下の過程となります。
- 分子同士が衝突する
- エネルギーの高い状態となる
- 結合が切れ、新たな結合を作る
つまり、結合が切れなければいけません。しかしσ結合は強い結合のため、簡単には結合が切れません。単結合のみで構成されるエタンは反応性が悪いと記しましたが、これはすべての結合がσ結合だからです。
一方、π結合はそれぞれの結合がゆるいです。π結合の結合エネルギーは低いため、少しエネルギーを与えるだけで結合が切れ、化合物同士が反応します。
π結合の説明をするとき、エチレン(エテン)やアセチレンが頻繁に利用されます。エタンは単結合だけの化合物ですが、エチレン(エテン)には二重結合があります。アセチレンは三重結合があります。
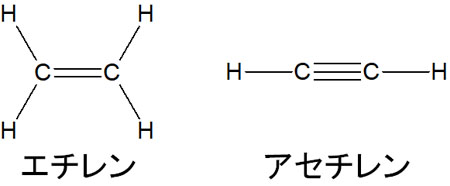
二重結合や三重結合を有することから、エチレンやアセチレンはπ結合があります。σ結合に比べて、π結合は結合がゆるいです。そのためエタンは反応性が悪いものの、エチレンやアセチレンは反応性が高い化合物で知られています。
単結合の化合物は安定な状態であっても、二重結合や三重結合は不安定になりやすいです。これは共有結合の中でも、π結合が強い結合ではないからです。
ベンゼン環や二酸化炭素など、π結合のすべてが弱い結合ではない
一般的には、π結合は弱い結合と考えればいいです。二重結合や三重結合があると反応性が高くなるのです。
ただ、二重結合を有する化合物(π結合をもつ化合物)のすべてが弱い結合というわけではありません。例えば、ベンゼン環は二重結合によってつながっています。つまり、π結合を有しています。
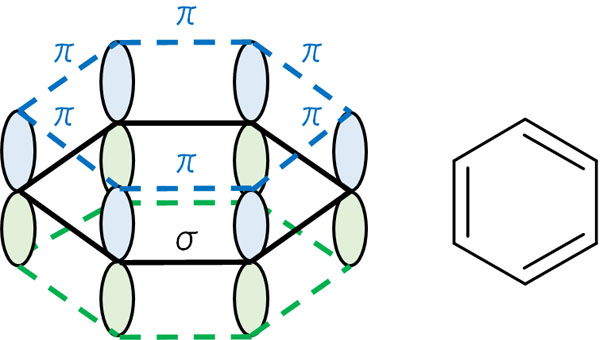
ただベンゼンでは、電子がベンゼン環のあらゆる部分に存在することになり、安定した構造を取ります。そのため、エチレンやアセチレンのように反応性が高いわけではありません。
また、二酸化炭素はO=C=Oという構造です。二重結合があるため、σ結合だけでなく、π結合を有する分子です。ただ二酸化炭素は安定な分子であり、二酸化炭素を化学反応させるためには大きなエネルギーが必要になります。
π結合を有する化合物のすべてで反応性が高いわけではありません。ただπ結合の性質を理解したとき、一般的にはπ結合のある化合物(二重結合や三重結合のある有機化合物)は反応性が高いと考えればいいです。
共有結合の種類と違いを学ぶ
分子が結合するとき、多くは共有結合によって結びつきます。これら共有結合には種類があり、σ結合(シグマ結合)とπ結合(パイ結合)の2つがあります。
どの原子であっても、電子軌道を重ね合わせることで、最初はσ結合を作ります。人と握手をするとき、必ずあなたは手を相手に差し出します。それ以外に選択肢はなく、これは分子の結合も同じです。単結合はどれもσ結合と理解しましょう。
一方で二重結合や三重結合を作るとなると大変です。原子の手は人間と違い、腕を自由に動かすことはできません。そこで結合軸に対して垂直に腕を伸ばし、頑張って相手と手をつなぐ必要があります。その結果、σ結合に比べて弱い結合になります。これがπ結合であり、エチレンやアセチレンが例として頻繁に利用されます。
ここでは、分かりやすくσ結合やπ結合を解説しました。共有結合には種類があることを理解して、σ結合とπ結合の特徴を学びましょう。






