新たな炭素鎖を作る方法として、エノラートを利用した合成反応があります。エノラートによる有機化学合成の一つがクライゼン縮合です。
クライゼン縮合では、エステルをもつ分子とエノラートが反応します。その結果、新たなカルボニル化合物を得られます。またクライゼン縮合が分子内で起こる場合、ディークマン縮合(分子内クライゼン縮合)と呼ばれます。
重要な有機化学反応の一つがクライゼン縮合です。ただ、クライゼン縮合では利用する塩基や反応機構など、事前に理解しなければいけないことがあります。
目的化合物を得るためには、正しい試薬を選択し、反応条件を検討しなければいけません。ここでは、クライゼン縮合の反応機構や注意点を解説していきます。
もくじ
エノラートとエステルの反応がクライゼン縮合
2つのエステルを反応させる縮合反応がクライゼン縮合です。クライゼン縮合はエノラートによる合成反応の一つです。
エステルを含め、カルボニル基をもつ化合物では、塩基によってα炭素の水素原子(α水素)が引き抜かれやすいです。その結果、ケト型からエノール型の化合物へと変化します。
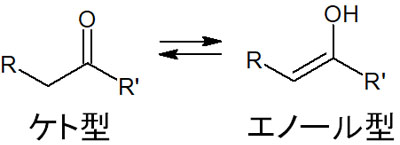
塩基によって、エノール型の分子になります。このとき塩基によって生成されるエノール型の化合物がエノラートです。エステルに塩基性試薬を加えることで、以下のようにエノラートを合成できます。
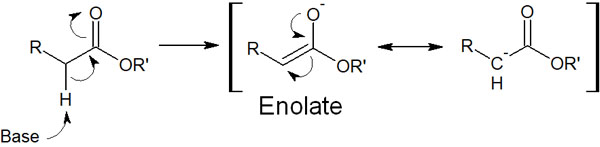
エノラートの炭素原子はマイナスの電荷を帯びています。いわゆるカルボアニオン(カルバニオン)であるため、エノラートは求核性が高いです。そのため他のカルボニル炭素に攻撃し、新たな炭素結合を作ることができます。
以下のような作用機序にて、エノラートはエステルに求核攻撃します。
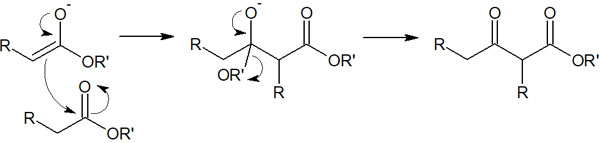
カルボニル炭素は求核攻撃を受けやすいことで知られています。そのため、エノラートがエステルに求核攻撃することで反応が進行します。
その後、酸素原子の電子が戻ると同時に、エステルが脱離します。水またはアルコールが脱離することで新たな分子を形成することを縮合といいます。この反応は縮合の一種であり、ドイツの化学者であるクライゼンによって発見されたため、クライゼン縮合という名前です。
・アルドール反応との違いは何か?
なお、クライゼン縮合と似た合成反応にアルドール反応があります。アルドール反応も同様に、エノラートによって合成反応が進行します。
クライゼン縮合では、エノラートとエステルが反応します。一方のアルドール反応では、ケトンまたはアルデヒドに対してエノラートが反応します。エノラートと反応する化合物がエステルなのかケトン(またはアルデヒド)なのかによって、合成反応の名称や生成物が変わります。
またクライゼン縮合では1当量の塩基が必要です。一方のアルドール反応では、触媒量の塩基で反応が進むという違いもあります。
β-ケトエステルは酸・塩基反応によってエノラートになる
それではクライゼン縮合によって化合物が生成された後、ケトンはエノラートによって攻撃を受けないのでしょうか。
クライゼン縮合によって合成された化合物をβ-ケトエステルといいます。エステルに比べて、ケトンのほうが求電子性は高いです。そのため、エノラートはエステルではなく、β-ケトエステルのケトンに対して求核攻撃するように思えます。
ただ実際には、生成物のケトン(β-ケトエステル)とエノラートが反応することはありません。これは、β-ケトエステルのα炭素の酸性度が高いからです。
クライゼン縮合は塩基性条件で合成反応させます。強塩基が存在することで、エノラートが生成するのです。溶液中に塩基が存在するため、β-ケトエステルのα炭素に結合している水素原子(α水素)は塩基によって引き抜かれます。その結果、以下のような安定なエノラートイオンとなります。
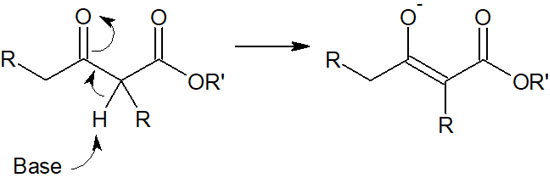
塩基によってβ-ケトエステルから形が変わった結果、エノラートによる求核攻撃を受けることはなくなります。そのため、クライゼン縮合ではβ-ケトエステルとエノラートが反応することはありません。
なお、反応を止めるときは塩酸などの酸性溶液を加えます。酸・塩基反応より、β-ケトエステルの形に戻ります。
分子内縮合による環化はディークマン縮合と呼ばれる
なお、分子内にエステルが2つ存在する場合、分子内クライゼン縮合が起こることで環化します。この反応をディークマン縮合といいます。
反応機構はクライゼン縮合とまったく同じです。ただ、2つのエステル分子が縮合するのか、分子内で縮合するのかによって反応の名前が変わります。
ディークマン縮合が起こる条件としては、環化して生成する化合物が5員環または6員環のときです。4員環や7員環では、立体化学でのひずみが大きいため、ほぼ反応は進行しません。ディークマン縮合では、生成物が5員環または6員環になると理解しましょう。
この条件を満たす場合、以下のような反応機構によってディークマン縮合が進行します。
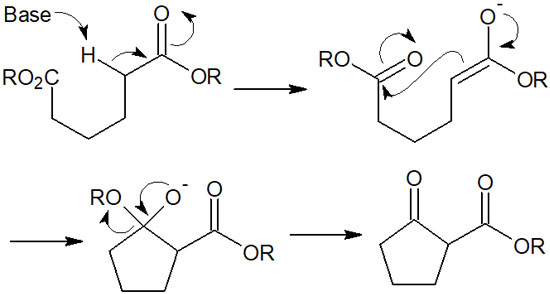
クライゼン縮合の反応機構を学んでいる場合、ディークマン縮合を理解するのは簡単です。塩基性条件にて、分子内反応での環化でβ-ケトエステルを合成できます。
・ハロゲン化アルキルでのアルキル化が可能
なお前述の通り、塩基性条件で反応させるのでβ-ケトエステルは安定なエノラートとして存在しています。そのため、酸を加える前にハロゲン化アルキルと反応させることで、アルキル化することができます。
例えば、以下のようになります。
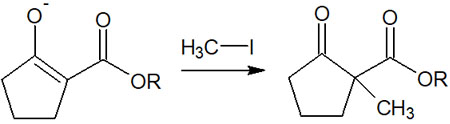
安定なエノラートなので反応性は低くなっているとはいっても、炭素原子がマイナスの電荷を帯びているため求核性があります。そのためクライゼン縮合(またはディークマン縮合)による反応を進めた後、アルキル化によって炭素鎖を作ることが可能です。
2種類の分子で起こる交差クライゼン縮合
なおクライゼン縮合では、同じ分子同士でクライゼン縮合させる例によって、化学反応が説明されます。それでは、異なる2種類の分子でクライゼン縮合させることはできないのでしょうか。違う分子を用いてクライゼン縮合させる合成を交差クライゼン縮合といいます。
交差クライゼン縮合では、以下の反応が利用されます。
- エステルとエステルの反応
- エステルとケトンの反応
ケトンについても、エノラートを生成することが知られています。そのためエステル同士で交差クライゼン縮合させるだけでなく、エステルとケトンで反応させることもできます。例えば、エステルとケトンでは以下のような反応機構になります。
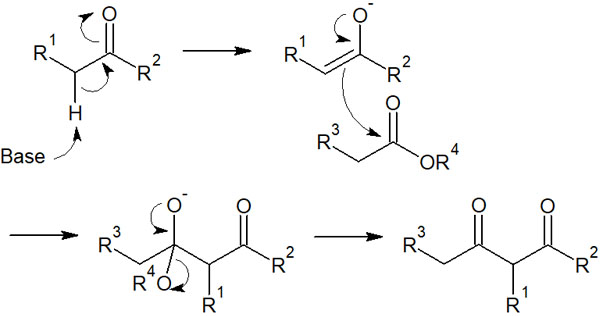
エステル同士のクライゼン縮合では、β-ケトエステルが合成されます。一方でエステルとケトンの交差クライゼン縮合では、β-ジケトンの化合物を合成できます。
一方のα位に水素原子がないと交差クライゼン縮合が効果的
ただ、交差クライゼン縮合をするときは注意点があります。それは、α水素のないエステルを利用することです。
エノラートを得るためには、分子にα水素がなければいけません。α炭素に結合しているプロトンが引き抜かれることで、エノラートが合成されます。ただ、反応させる化合物の両方ともα水素があると、いろんな種類のエノラートが生成され、複雑な反応になります。
そこで、塩基によって引き抜かれるα水素が一ヵ所だけになるエステルを反応させる必要があります。例えば、以下のエステル同士の反応ではα水素は一ヵ所だけです。
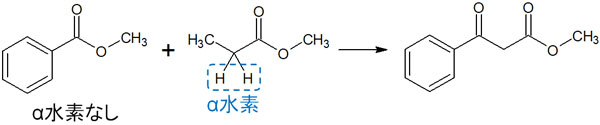
交差クライゼン縮合では、一方のエステル(またはケトン)にα水素がない場合に有効です。反応させる化合物にα水素がいくつもある場合、複雑な合成反応になってしまいます。そのため、交差クライゼン縮合では反応させるときの条件が限られます。
水酸化ナトリウムの利用でカルボン酸となり、脱炭酸できる
なお、クライゼン縮合で利用する塩基として水酸化ナトリウム(NaOH)を利用することは基本的にありません。
水酸化ナトリウムを利用することで、エノラートを合成することが可能です。それにも関わらず、なぜNaOHはクライゼン縮合でほとんど利用されないのでしょうか。この理由は、OH–がエステルを攻撃することでカルボン酸が合成されるからです。
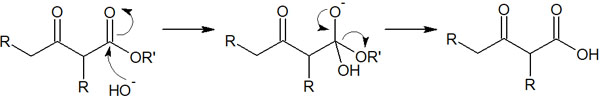
このように、カルボン酸の3位にカルボニル基(ケトン)をもつ化合物が合成されます。
ちなみに、3位にケトンがあるカルボン酸を加熱すると脱炭酸します。化合物が分解し、カルボン酸が二酸化炭素として放出されます。以下のような反応機構によって脱炭酸します。
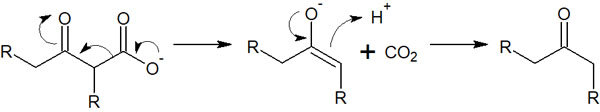
クライゼン縮合をした後、カルボン酸を得たかったり、脱炭酸したかったりする場合、水酸化ナトリウムを利用するといいです。ただ、そうでない場合はNaOHを塩基として利用することはありません。
ナトリウムメトキシド、ナトリウムエトキシドでエステル交換する
それでは、その他の塩基なら何でもいいので利用すればいいのかというと、そういうわけではありません。例えば、塩基としてはナトリウムメトキシドやナトリウムエトキシドなどが知られています。
ただ、強塩基としてアルコキシドを利用する機会は少ないです。ナトリウムメトキシドやナトリウムエトキシドを利用すると、エステル交換によってメトキシドやエトキシドが生成されるからです。以下のようになります。
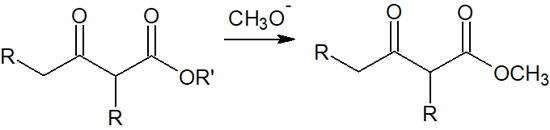
エステルにアルコールを加えると、エステル交換することは広く知られています。エステル交換が起こるため、塩基でナトリウムメトキシドやナトリウムエトキシドを利用することはほとんどありません。
・LDAやNaHの利用が一般的
それでは、クライゼン縮合ではどのような塩基を利用するのでしょうか。クライゼン縮合に限らず、エノラートを合成するときはLDA(リチウムジイソプロピルアミド:Lithium diisopropylamide)やNaH(水酸化ナトリウム)などの塩基が頻繁に利用されます。
LDAは以下のように、かさ高い塩基です。
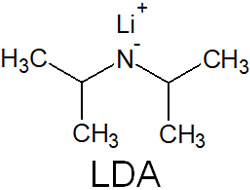
立体障害が大きいことから、LDAは求核性がほぼなく、塩基としてのみ働きます。またNaHも求核性がない強塩基です。エノラートを合成するとき、塩基の性質の違いを理解して、最適な塩基を利用すると考えましょう。
エノラートを利用し、クライゼン縮合させる
有機化学で新たな炭素結合を作るとき、エノラートを利用する化学反応は重要です。エノラートを利用した合成には、アルドール反応やマイケル付加などが存在し、その中の一つがクライゼン縮合です。
他の合成反応との違いとしては、エステルを利用することがあげられます。エノラートとエステルを利用した合成反応がクライゼン縮合です。なお、分子内クライゼン縮合による環化ではディークマン縮合という名前になります。
クライゼン縮合では、異なる分子を利用する交差クライゼン縮合も可能です。ただα水素がない分子を利用する必要があるなど、利用場面は限られます。
さらに、利用する塩基を考えましょう。塩基によっては副反応を起こすため、目的化合物を得るために最適な塩基を選択しなければいけません。これらを理解することで、クライゼン縮合によって目的化合物を得られます。