有機化合物の中でも、ヒドロキシ基(-OH)を有する化合物はアルコールと呼ばれています。一般人にとってアルコールはエタノールを指し、多くの人がエタノール入りの飲料を飲むことで酔います。ただ有機化学では、ヒドロキシ基を有する化合物を含めてアルコールと表現します。
アルコールを有する化合物は非常に多く、アルコールからさまざまな化合物へと合成することができます。また反応させる試薬を変えることで、生成物が違ってきます。
アルコールの反応では、主に以下の合成反応がメインになります。
- 酸化
- 塩基性条件での反応
- 酸性条件での反応
それぞれ別の合成反応になるため、反応機構は異なります。ただアルコールを利用して多種多様な化合物の合成が可能になるため、それぞれの反応機構を理解する必要があります。
もくじ
酸化反応では第一級、第二級、第三級で生成物が異なる
アルコールで最初に考えるべき合成反応は酸化です。アルコールを酸化させることで、アルデヒドやカルボン酸、ケトンを合成できるようになります。つまり、アルコールから他の官能基を合成することができます。
どのような官能基を合成できるのかについては、炭素に結合している置換基の環境で異なります。また、どのような試薬を用いるのかによっても変わってきます。
そうしたとき、アルコールが酸化するとき第一級や第二級、第三級によって生成物が異なります。以下のようになります。
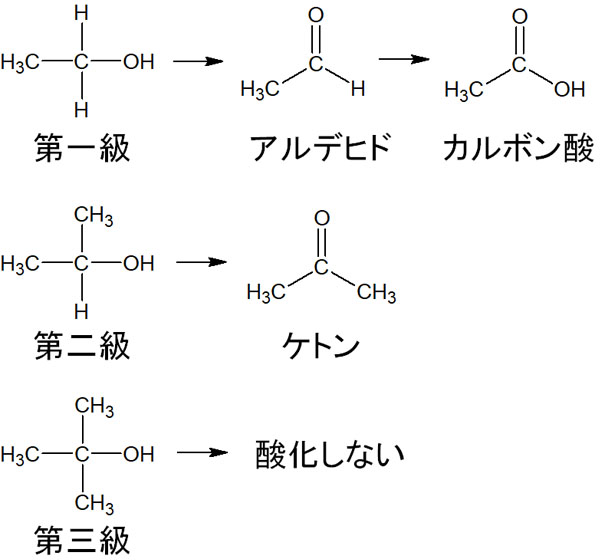
炭素原子にアルキル鎖がどのように結合しているのかによって、酸化反応によって生成される化合物がこのように違ってきます。なお第三級アルコールは酸化されません。アルコールであれば必ず酸化されるわけではありません。
クロム酸や次亜塩素酸の酸化でカルボン酸やケトンを合成する
アルコールが酸化反応をするとき、酸化剤を利用しなければいけません。酸化剤としては、クロム酸や次亜塩素酸などが有名です。利用する酸化剤としては、クロム酸でも次亜塩素酸でも、どちらでもいいです。これらを利用することで、アルコールを酸化できます。
なお6価のクロムは毒性が高く、合成反応後の廃液処理には注意しなければいけません。次亜塩素酸については、塩素系漂白剤の主成分になります。
クロム酸や次亜塩素酸を利用すると、以下の化合物を得られます。
- 第一級アルコール:カルボン酸
- 第二級アルコール:ケトン
第二級アルコールは酸化によってケトンしか合成されません。一方で、第一級アルコールの酸化でアルデヒドを得ることはできるのでしょうか。これについて、クロム酸や次亜塩素酸による酸化でアルデヒドを得ることはできません。アルデヒドが生成された後、すぐにカルボン酸が生成するからです。
そのためアルコールの一般的な酸化反応では、カルボン酸またはケトンを得ることができます。
アルデヒド生成やカルボン酸合成の反応機構:ジョーンズ酸化
それでは、アルコールを酸化するときどのような反応機構によってカルボン酸が合成されるのでしょうか。アルデヒドやカルボン酸の合成機構のほうが複雑なので、カルボン酸の生成メカニズムを理解できれば、どのようにケトンが合成されるのかについて理解できるようになります。そこでケトンではなく、ここではカルボン酸を得るまでの反応機構を記します。
アルコールを酸化し、カルボン酸やケトンを得る合成反応は人名反応でもあります。ジョーンズ酸化と呼ばれており、CrO3やH2CrO4などのクロム酸を利用します。水溶液中で反応させる合成反応であり、以下のような反応機構によってアルデヒドが合成されます。
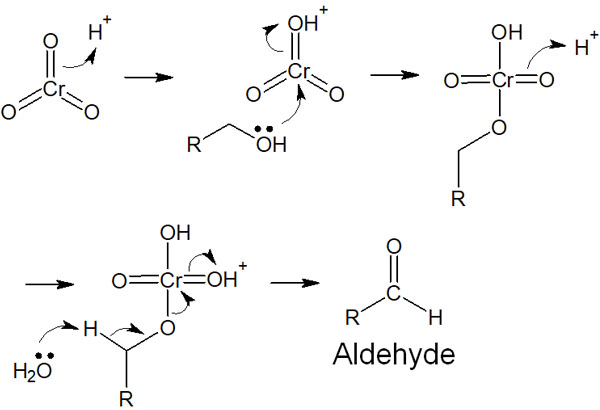
ジョーンズ酸化の反応機構は少し複雑ですが、水溶液中でクロム酸が化合物を酸化することでアルデヒドが合成されます。第二級アルコールの場合はケトンが生成されますが、同じ反応機構になります。
それでは、クロム酸を用いたジョーンズ酸化で第一級アルコールがカルボン酸まで合成されるとき、どのような反応機構になるのでしょうか。
水が存在する場合、アルデヒドは水と水和反応を起こします。その結果、ジェミナルジオール(gem-ジオール)が生成されます。反応機構は以下になります。
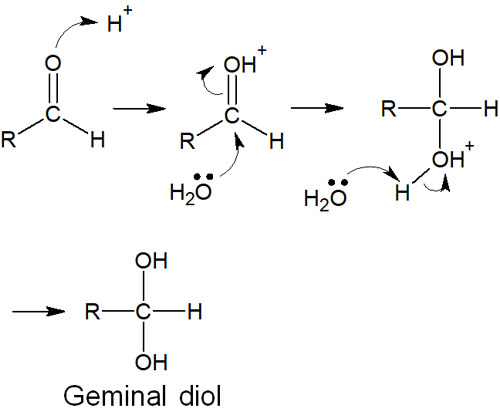
いずれにしても、水が存在することで水和反応が進行し、アルデヒドは2つのヒドロキシ基を有する化合物(gem-ジオール)に変化します。
その後、ジェミナルジオールは再びクロム酸と反応することでカルボン酸へと酸化されます。
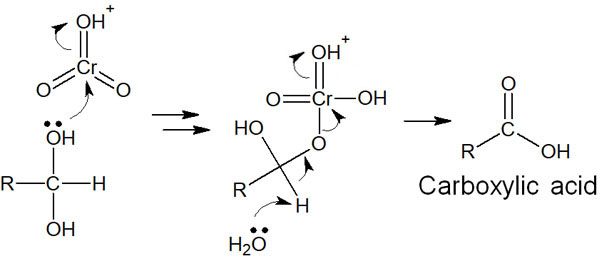
重要なのは、ジョーンズ酸化では水が存在するため、アルデヒドが生成した後に水和し、-OHが生成されることにあります。その結果、カルボン酸が合成されます。
PCCやSwern酸化(スワーン酸化)による無水条件でのアルデヒド合成
このようにクロム酸を用いたジョーンズ酸化によって、カルボン酸やケトンを得ることができます。それでは第一級アルコールを酸化させるとき、カルボン酸まで進むのではなく、アルデヒドの合成でストップさせることはできないのでしょうか。
方法によっては、アルコールの酸化でアルデヒドを合成することが可能です。やり方としては、無水状態で酸化反応を進めます。
前述の通り、ジョーンズ酸化では水が存在する条件下で合成反応を進めます。水があるため、アルデヒドは水和することでジェミナルジオール(gem-ジオール)となり、カルボン酸まで酸化反応が進みます。つまり水が存在しなければ、水和することはなくカルボン酸は生成されません。
そこで、無水条件下での酸化反応を可能にした合成反応試薬としてPCC(クロロクロム酸ピリニジウム)があります。以下がPCCの構造式です。
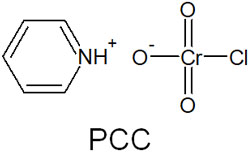
PCC(クロロクロム酸ピリニジウム)と第一級アルコールを反応させるとき、反応機構は以下のようになります。
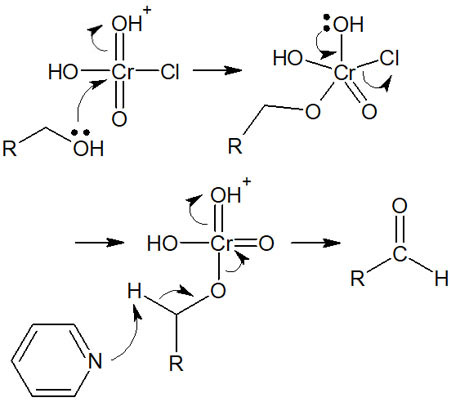
アルデヒドを得た後、反応はここでストップします。水が存在しないため、アルデヒドからカルボン酸へと酸化されることはありません。
・Swern酸化(スワーン酸化)での合成
なおアルデヒドを得る有機合成反応ではSwern酸化(スワーン酸化)も用いられます。人名反応の一つがSwern酸化であり、PCCと同じく無水条件で第一級アルコールを酸化し、アルデヒドを得ることができます。
-78℃などの低温で反応させることにより、不要な副生成物が少なく合成反応を進められるのがSwern酸化です。有機化学では頻繁に活用される合成手法の一つです。
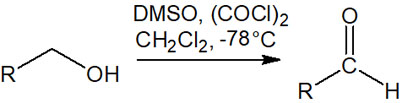
要は、無水条件下ではこのように「第一級アルコールを酸化して、アルデヒドを得られる」と理解すればいいです。なお第二級アルコールに対してPCCやSwern酸化(スワーン酸化)を行うと、ケトンを得ることができます。
金属ナトリウムで塩基(求核剤)として働くアルコール
このように、使用する酸化剤や合成条件を変えることで、得られる最終生成物が異なります。一方でアルコールの酸化ではなく、他の有機合成反応ではどうなるのでしょうか。
一般的にアルコールは中性の物質として知られています。メタノールもエタノールも中性です。ただ有機化学では、酸と塩基の関係で考える必要があります。強力な塩基と共存させることによって、アルコールは塩基(求核剤)として利用できます。
アルコールは酸素原子が存在しており、電気陰性度が高いです。そのため分子内で分極しており、強力な塩基が存在するとH+を放出し、アルコキシドイオンになります。多くのケースでアルカリ金属が利用され、アルコールに結合しているH+を引き抜くようにします。
アルカリ金属で最も一般的なのはNa(ナトリウム)です。試薬として水素化ナトリウム(NaH)を加えることで、アルコールにある水素(プロトン)が引き抜かれてイオン化します。こうして、アルコキシドとして強塩基(強い求核剤)が生成されます。
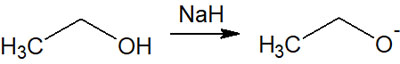
塩基による有機合成では、求核置換反応(SN1反応とSN2反応)が頻繁に利用されます。求核剤として、アルコキシドイオンが他の分子を攻撃することで求核置換反応を起こすのです。
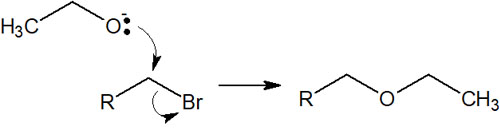
エーテルを合成したい場合、アルコールを用いた求核置換反応は非常に重要です。
酸触媒による置換反応・脱離反応
一方で、アルコールのOHは他の置換基と置き換わることもできます。つまりOHが脱離し、その代わりとして他の置換基と入れ替わると理解しましょう。
先ほど、アルコールを塩基として活用することで求核置換反応を起こすことを説明しました。このときはSN1反応またはSN2反応が起こります。アルコキシドイオンが求核攻撃し、脱離基と置き換わります。そうではなく、OHが脱離基になります。
ただそのままの状態では、OHが脱離基になることはありません。そこで、酸触媒を利用します。強酸を利用することで、酸素原子に水素(プロトン)が結合して、-OHは-OH2+になります。-OH2+は優れた脱離基であるため、置換反応や脱離反応を起こすことができます。
例えばアルコールと塩化水素(HCl)を反応させることで、ヒドロキシ基はクロロ基に置き換わります。
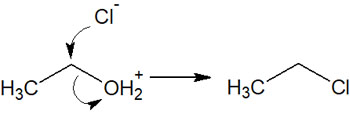
第一級アルコールであれば、SN2反応で反応が進行します。一方で第二級アルコールや第三級アルコールでは、SN1反応で反応が進行します。いずれにしても求核置換反応によって-OH2+が脱離し、ハロゲンと置き換わります。
ハロゲン化させるさまざまな方法
ただ、HCl(塩化水素)やHBr(臭化水素)をアルコールに加えただけの状態では、反応が進行しないことがよくあります。そのため、通常は塩化チオニル(SOCl2)や三臭化リン(PBr3)などの試薬を用いてハロゲン化します。
アルコールに塩化チオニル(SOCl2)や三臭化リン(PBr3)を加えることで、アルコールはハロゲン化します。例えば塩化チオニルを利用する場合、以下のような反応機構になります。
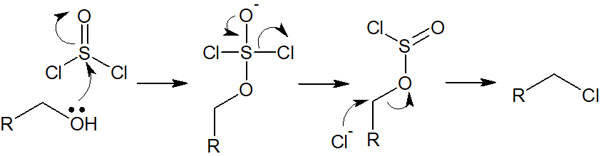
酸塩化物を加えることで、このような反応機構によって合成反応が進行していきます。
それでは、なぜアルコールをハロゲン化するのでしょうか。アルカンに結合しているハロゲンは脱離基として優れており、アルコールやアミンなどと求核置換反応を起こします。そのため以下のような結合を新たに作ることができます。

酸触媒(酸塩化物)を活用してハロゲン化しただけで合成反応が終わることは少ないです。その後に再び反応させることで、目的化合物を得ることができます
いずれにしても、ハロゲン化することで、ハロゲン化アルキルを合成できることを理解しましょう。ハロゲン化アルキルを利用して、次の合成反応を進めるのです。
・スルホン酸エステルの利用もよくある
なおアルコールのハロゲン化を説明しましたが、アルコールをスルホン酸エステル化することもよくあります。スルホン酸エステルは以下のような構造式をしています。
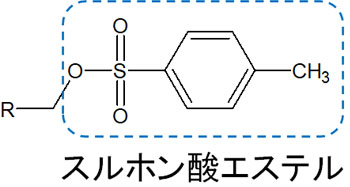
ハロゲンと同じように、スルホン酸エステルは非常に優れた脱離基として機能します。そのため求核置換反応によって、新たな結合を作ることができます。
反応機構はハロゲン化アルキルと同じです。スルホン酸エステルを合成後、求核剤を加えることで置換反応させます。
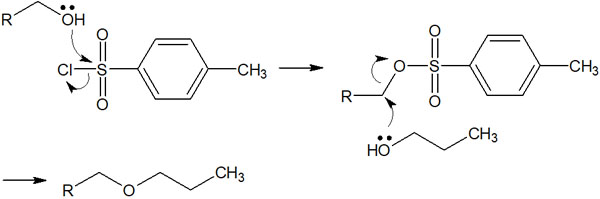
重要なのは、アルコールは優れた脱離基へ変換できるという事実です。その後、試薬を加えることで置換反応が起こり、新たな化合物を合成できるようになります。
アルコールの合成反応は種類がある
官能基によって性質が異なるため、どのような合成反応が可能なのかについて理解しなければいけません。その中でもアルコールは主な反応が決まっています。
酸化反応と求核置換反応がアルコールにとってメインの合成反応です。酸化反応については、利用する試薬や合成環境によって生成物が異なることを理解しましょう。
一方で求核置換反応では、塩基条件なのか酸条件なのかによって反応の内容が変わります。強塩基と一緒にすると、アルコールはアルコキシドイオンになって求核置換反応を起こします。それに対して、酸触媒の環境では置換反応によってヒドロキシ基が他の置換基に置き換わります。
アルコールの合成反応では、これらの特徴があります。それぞれの反応機構は異なりますが、頻繁に利用する合成反応ばかりなので、どのようにアルコールが反応するのかについて理解するようにしましょう。






