化合物の構造決定をしたり、どのような化合物が含まれているのかを検出したりするとき、非常に優れた手法に質量分析法(MS)があります。
既知化合物を測定するとき、質量分析法を利用すれば高確率でターゲット化合物かどうかを判断できます。未知化合物であったとしても、質量分析法を利用することで分子量を測ることができます。そこから、分子の構造を推測できます。
有機化学でも生化学でも、非常に多くの研究者が利用する分析装置がMSです。そのため、質量分析法をどのように活用するのかについて理解しなければいけません。
また、MSの原理を理解するのは当然として、スペクトルデータの読み方を学ぶ必要があります。これによりターゲット化合物の分子量を測り、構造式を推測できるようになります。どのように質量分析法を利用すればいいのか、ここでは解説していきます。
もくじ
化合物の分子量を測定するのが質量分析法
分析手法の中でも、質量分析では何を測定するのでしょうか。質量分析法では、化合物の分子量を測ります。
- 未知の天然化合物を抽出した
- 食品への混入物の成分を知りたい
- ターゲット化合物が生成されたか不明
これらの事態に陥ることはよくあります。そこで、質量分析法を利用します。MSを利用することで分子量が分かれば、どのような物質が含まれているのか不明であったとしても、含まれている物質を推測できます。
もちろん複数化合物が存在する状態ではなく、ターゲット化合物が一つだけ存在する状態で試料をセットし、測定する必要があります。そのため事前にクロマトグラフィーなどで物質を単離し、測定することで、目的化合物の分子量を得られます。
磁場を活用し、化合物の質量を測定する
なぜ、MSを利用すれば測定物質の分子量が分かるのでしょうか。これは、イオン化した物質を磁場で測定するからです。
物質をイオン化する方法はいくつかあり、最適な方法によって物質をイオンにします。イオンになった分子は電荷を帯びるようになります。質量分析法では、分子はプラスのイオンとなります。
その後、磁場をかけます。磁場の中をイオンが通ると、イオンは曲がります。磁場の強さが違えば、イオンの曲がり具合は異なります。より正確にいうと、分子量が大きい(重い物質)であるほど、強力な磁場をかけなければ曲がりません。
強い力を加えないと重いものを動かせないのは、私たち人間でも磁場でも同じです。
そこで磁場の力を少しずつ変えていき、検出器に計測されるかどうかを確認します。最適な磁場でない場合、途中の壁に当たって検出器まで到達せず、何も観察されません。一方、最適な磁場であれば分子を観測できます。
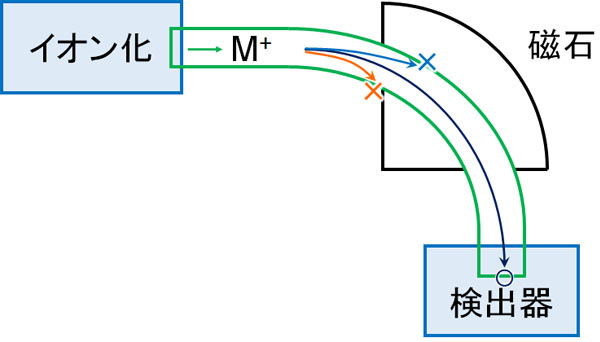
磁場を少しずつ変えていき、イオン化された分子が検出されるかどうかを確認することで、ターゲット化合物がどのような分子量なのかを測定できるようになっています。
こうして得られるMSでのスペクトルをマススペクトルといいます。質量分析法で観察されるスペクトルデータを見ることで、ターゲット化合物がどのような物質なのかを推測できるようになります。
多くは電子イオン化が質量分析法で利用される
これら質量分析法では、さまざまなやり方が存在します。以下のように種類があります。
- 電子イオン化法(EI)
- 化学イオン化法(CI)
- 高速原子衝撃法(FAB)
- マトリックス支援レーザー脱離イオン化法(MALDI)
- エレクトロスプレーイオン化法(ESI)
試験勉強する学生でない限り、これらの細かい特徴を理解し、覚える意味はありません。そのため、それぞれの分析手法について細かく特徴を記すことはしません。いずれにしても、質量分析法にはいくつかの方法があると理解すればいいです。
MSの中でも、最も一般的な手法が 電子イオン化法(EI)です。加熱することでイオン化させ、分子量を測定する手法です。測定したい試料に電子をぶつけることでイオン化させます。ターゲットの化合物だけを測定するため、簡便でありデータ解析が容易です。
ただ 電子イオン化法(EI)では、熱に弱い化合物や、タンパク質など高分子化合物は測定できません。その場合、他の分析手法によって分子量を計測します。
MSでのスペクトルデータの事例と読み方:質量電荷比(m/z)と電荷(z)
それでは、MSでマススペクトルを測定したとき、読み方はどのようになるのでしょうか。質量分析をするとき、一つのピークが検出されるわけではありません。マススペクトルでは、複数のピークを観察できるようになります。
例えば、酢酸をMSで計測したときのマススペクトルのデータは以下になります。
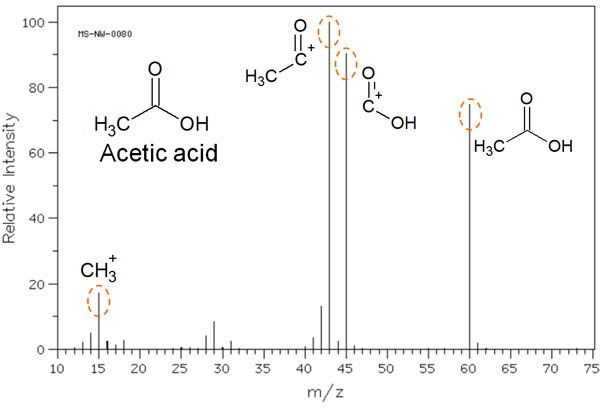
このように、いくつものピークが観察されることが分かります。
分子をイオン化するとき、必ずしも酢酸のままイオン化するとは限りません。分子が開裂することで、上の図に記した分子が生まれます。その結果、これらの分子がマススペクトルで検出されます。
横軸は質量電荷比(m/z)で表します。mはイオンの質量であり、zは電荷を表します。要は、m/zが分子量のことを記していると理解しましょう。
一方で縦軸はイオン強度です。マススペクトルの中で、最も多く観測されるピークが100%となります。先ほどの図でも、最もピークが検出された分子(m/z 43)については、縦軸のイオン強度が100%です。これに比べて、どれだけマススペクトルで検出されたのか比率を縦軸で表しています。
酢酸を事例にして、マススペクトルの読み方を解説してきました。マススペクトルではターゲット化合物の分子量だけでなく、電子をぶつけることで生じる他の分子も複数生成されるため、そこから構造式を推測できるようになっています。
ラジカルカチオンによる開裂で分子が分かれる
それでは、マススペクトルで検出される分子としてはどのようなものがあるのでしょうか。高エネルギーの電子ビームを当てることで、分子に存在する電子をはじき出し、ラジカルカチオンを作りだすのが質量分析法です。
電子が飛んでいくことで、不対電子を生じます。正電荷を帯びたラジカルカチオンになったとき、特に反応を起こさずに検出されれば、ターゲット分子の分子量が計測されます。
ただ、ラジカルカチオンは反応性が高いです。例えば酢酸では、先ほどの記したように、いくつもの分子が検出されます。
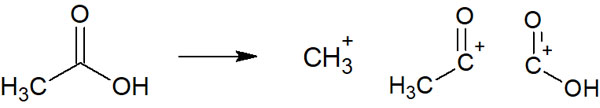
多くの場合、MSによって高エネルギーの電子ビームを当てたとき、非共有電子対(結合に関与していない電子)が外へはじき出されるようになります。例えば、窒素原子や酸素原子が構造式の中にあると、これら窒素原子や酸素原子の非共有電子対がはじき飛ばされ、ラジカルカチオンを生じやすいです。
そのためアミノ基(NH2)やカルボニル基(C=O)などの構造式があると、その部分で結合が切れやすくなります。
他には、ベンゼン環に結合した塩素原子や臭素原子、ヨウ素原子などは高エネルギーの電子が当たることで、これらの原子が飛んでいきやすいです。
なお、必ずしもラジカル開裂をするわけではなく、その他の反応機構によって分子の結合が切れることもあります。転位反応により、分子の形が大きく変わることもあります。ただ最も多いのが、ラジカル開裂による反応です。ラジカル開裂が起こることで、マススペクトルに複数のピークが観測されます。
塩素や臭素など、同位体が検出される
MSでの測定をするとき、他に考えなければいけないのが同位体です。例えば炭素原子は12Cが一般的です。ただ少ないながらも、13Cの炭素が存在します。これら同位体は質量が異なります。そのため、質量分析法で検出されるピークも異なります。
13Cは割合が少ないです。しかし、塩素と臭素は高い割合で同位体が存在します。以下のような割合になります。
- 35Cl:37Cl = 3:1
- 79Br:81Br = 1:1
そのため構造式の中に塩素原子や臭素原子を有する場合、同位体ピークがはっきりと検出されます。例えば、以下のようになります。
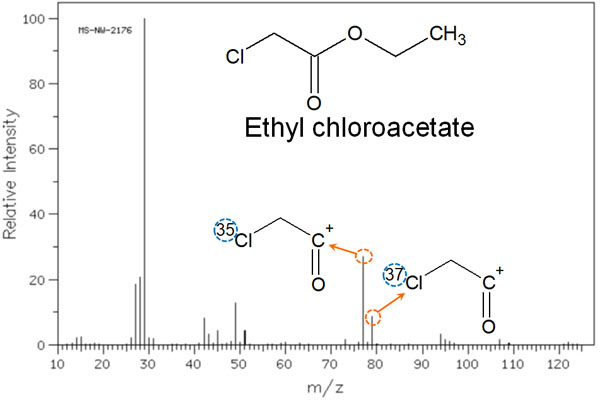
塩素原子の場合、同位体は先ほど記した通り3:1の割合で観測されます。そのため縦軸のイオン強度についても、3:1の割合でスペクトルピークが表れます。
M+1で炭素原子の同位体ピークが観察される
先ほど説明した通り、12Cに比べると、13Cの存在確率は低いです。存在比1.1%で13Cが存在します。それでは、MSによる分析をするとき13Cは無視してもいいのでしょうか。マススペクトルでは、必ずしも13Cを無視すればいいわけではありません。
分子量が低い場合、存在比1.1%のため、13Cはほぼ観測されません。ただ分子量が大きくなり、多くの炭素原子を有するほど、13Cの同位体ピークが観測されるようになります。本来の分子量はMで表されますが、13Cの同位体ピークはM+1で表されます。
n個の炭素原子を有する場合、M+と[M+1]+の強度比は以下になります。
- M+:[M+1]+ = 100:1.1×n
n個の炭素原子があれば、その分だけ13Cの炭素原子が観測される確率が高くなります。例えば、以下は4-アセチルビフェニルのマススペクトルです。
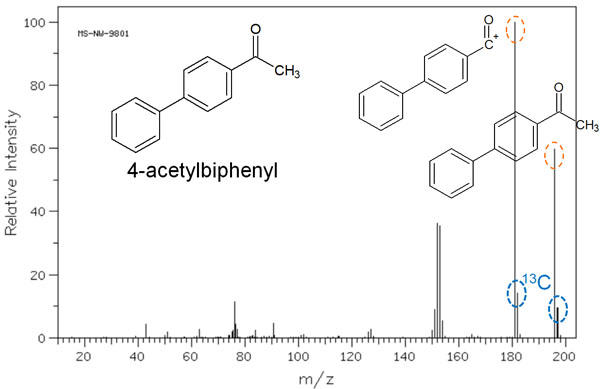
4-アセチルビフェニルの分子量は196です。ただマススペクトルでは、メインピークの隣に小さいピークが見えます。このピークは意味があり、13Cが同位体として観測されたからなのです。この分子は14個の炭素原子を有するため、「1.1% × 14個 = 15.4%」の強度で[M+1]+のスペクトルピークが観測されます。
研究をするときに同位体を意識する機会は少ないです。ただマススペクトルでは、炭素原子の同位体を強く意識する必要があります。
構造解析で重要なマススペクトル
分析手法の中でも、多くの研究で多用される手法の一つが質量分析法です。ターゲット化合物の分子量を測定することができ、未知化合物として何が含まれているのか推測することができます。有機化学でも生化学でも、広く利用される分析手法です。
分かるのは分子量だけではありません。ラジカルカチオンを生じるため、分子内で開裂し、その他のピークも観測されます。これらのピークから、分子の構造式を推測することが可能です。
磁場の強さによって分子量を測定する手法のため、原理は簡単です。ただいくつかの分析法があり、最も利用される電子イオン化法(EI)では、「熱に弱い分子は測定できない」という欠点があります。そこでMSをするとき、最適な方法を選ばなければいけません。
さらには、同位体を考慮することも重要です。これらの特徴を理解したうえで、科学実験で質量分析法を利用しましょう。






