化学系の研究者では、非常に多くの人で利用されているものにNMR(核磁気共鳴)があります。特に有機化学を専攻したり、化合物の構造決定が必要だったりする研究室では頻繁にNMRを利用します。
こうしたNMRでは、1H-NMRと13C-NMRが存在します。ただ主流は1H-NMRであり、13C-NMRを利用することは少ないです。難しい構造の化合物を研究しない限り、13C-NNRを利用することはないのです。つまり、最初は1H-NMRだけを学べば問題ありません。
それでは、1H-NMRはどのような原理になっているのでしょうか。核磁気共鳴によって化合物の構造式を調べるとはいっても、NMRは線が表れるだけであり、データを読み解く必要があります。
そこで、どのようにして1H-NMRを理解すればいいのか解説していきます。
もくじ
ゼーマン効果でエネルギーを生み出す意味
1H-NMRの原理について理解するためには、場について学ぶ必要があります。エネルギーの違いを生み出すためには、場が存在しなければいけないからです。
例えば、私たちが宇宙空間に移動するとします。この場合、どのような体勢であったとしてもエネルギーに違いはありません。宇宙空間では、重力が存在しないからです。地球では、重力が場になります。
場のある地球では、立っている状態と逆立ちを比較したとき、どちらのエネルギーが高いでしょうか。当然、逆立ちしている状態のほうが高いです。

ただ、地球ではなく月ではどうでしょうか。地球に比べて、月の重力が1/6です。つまり月では、場のエネルギーが低くなっています。このように場の力が異なれば、物質が保有するエネルギーも異なるようになります。
このとき電子は電荷をもっており、電子は回転しています。電荷を有する物質が回転すると、結果として磁力を発するようになります。そこで、ここに磁場をかけます。磁場をかければ、小さい磁石である電子は、2つの状態のみとなります。
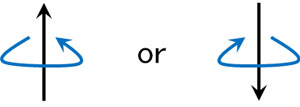
また小さい磁石である電子は、N極とS極を有するようになります。その結果、磁場があるとき「N極とN極が近くにある状態」だとエネルギーが高く、反対の状態ではエネルギーが低くなります。

このように、強い磁場の中では原子スペクトルが変化し、いくつものスペクトル(情報)を読み取れるようになることをゼーマン効果といいます。
磁場をかけることでゼーマン効果を生み出します。その結果、さまざまな方向を向いていた電子は2つの方向のみに分かれます。当然、エネルギーの小さいケースのほうが多いです。

こうしたゼーマン効果が起こっている状態で外部からエネルギーを与えると、すべて高エネルギーになるポイントがあります。
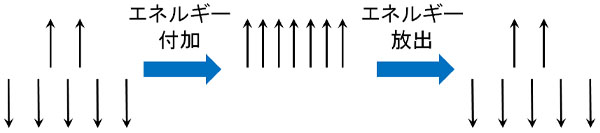
エネルギーを得た後、すぐにエネルギーを放出して電子は元の状態に戻ります。そこで、1Hプロトンが高エネルギーになったポイントがどこかを測定します。こうして、NMRデータとしてスペクトルが表れるというわけです。
電子密度(遮蔽効果)によって低磁場・高磁場の場所が異なる
ただ1Hプロトンを測定するとはいっても、水素原子の性質はどれも同じです。なぜ、表れるスペクトルに違いがあるのでしょうか。これは、それぞれの水素原子ごとに電子密度が異なるからです。NMR(核磁気共鳴)とは、水素原子の電子密度の違いを測定するツールだと理解しましょう。
例えば、水素原子に10のエネルギーを加えると、一瞬だけ高エネルギー状態になり、スペクトルを観測できるとします。このとき電子バリアーが3の状態だと、13のエネルギーを与えることでスペクトルを観測できます。
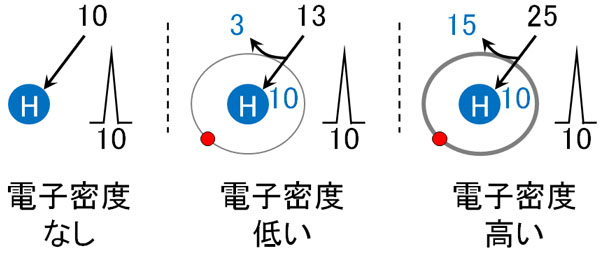
同様に考えると、電子バリアーが15の場合、25のエネルギーを与えればスペクトルを観測できます。電子のバリアーがエネルギーを遮ることを遮蔽効果といいます。
水素は炭素や窒素などの原子と結合しています。プロトン(水素原子)ごとに電子密度が異なるため、遮蔽効果により、どこにピークが観測されるのか変化します。
例えば、プロパノールの構造式は以下のようになります。
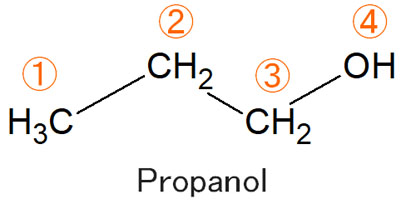
このとき2番目と3番目のプロトンでは、どちらが低磁場(低いエネルギー)で観測されるでしょうか。
2番目の水素原子だと、隣に炭素原子が2つあります。つまり電子が押されている状態であり、電子密度が高いといえます。
一方、3番目のプロトンは隣に酸素原子があります。酸素原子は電気陰性度が強く、電子は酸素原子側に引っ張られます。その結果、電子密度は低くなります。これらの事実から、3番目のプロトンは低磁場に表れると予想できます。
当然、酸素原子に直接結合している4番目のプロトンはより低磁場に観測されます。
簡単に考えれば、「水素原子(プロトン)の周辺の電子密度がどうなっているのかを調べる手法がNMR」と考えるようにしましょう。このときのスペクトルを確認することで、化合物の構造式を推測するというわけです。
低磁場・高磁場については、例えば以下のようにNMRのスペクトルが表示されます。
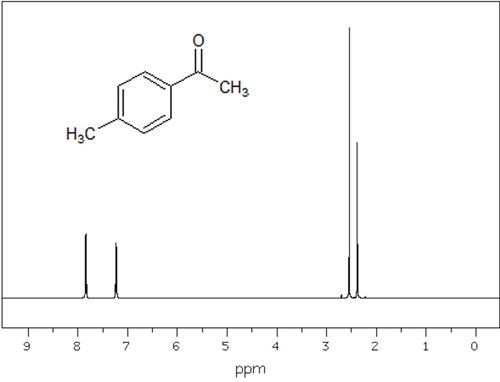
こうして、NMRで低磁場・高磁場のどこにピークがあるのかを確認します。化合物によってプロトンごとの電子密度が異なり、ピークの出現場所が違うというわけです。
NMRのシグナルで重要なカップリングと積分値
ただ、スペクトルが低磁場・高磁場のどこにあるのかを確認するだけでは、化合物の構造式を推測することはできません。NMRでは他にも考えなければいけないことがあり、それがカップリングと積分値です。
ピークが表れる場所に加えて、ピークの形や面積が重要になるというわけです。これらを調査するからこそ、化合物の構造を推測できるようになると考えましょう。
それぞれ、どのように考えればいいのか解説していきます。
ピークが割れるカップリング(非等価):シングレット・ダブレット
NMR(核磁気共鳴)の装置を利用するとき、通常だと、水素を観測したときは一つのシグナルとして観測されます。例えば、以下の状態では一つのピークのみ表れます。
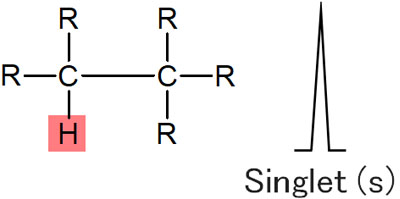
これをシングレットといいます。
しかし、NMRでは隣の炭素に結合している水素の影響を受けます。これをカップリングといいます。例えば以下の化合物で、赤色の水素原子に着目します。この場合、隣に水素原子が一つあるため、ピークは二重線になります。
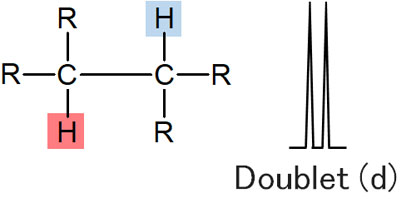
NMRでの二重線はダブレットといいます。
それでは、隣に水素原子が2つある状態ではどうでしょうか。この場合、ピークはさらに2つに割れ、四重線になります。
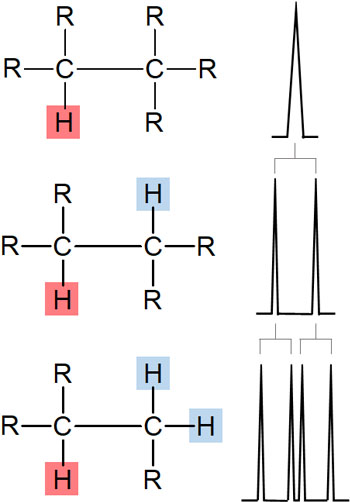
このように隣に水素原子がある場合、その影響を受けてピークが割れることを理解すれば問題ありません。
J値が等価な場合:トリプレット、カルテット、クインテット
ただ、通常の化合物は上記のようにピークが出現することはありません。先ほどは、非等価という特殊な状態を説明しました。そうではなく、等価な状態を考えるのが一般的です。
1H-NMRによってプロトンのピークが分かれるとき、ピークとピークの間の距離をJ値(カップリングコンシスタント:結合乗数)といいます。特別な理由がない限り、カップリングが起こったときのJ値は同じです。これを、等価な状態といいます。
それでは先ほどと同じように、「隣に水素原子が2つある状態」を考えてみましょう。J値は同じのため、カップリングすると真ん中のピークが重なるようになります。以下の図では、J値を12Hzと仮定しています。
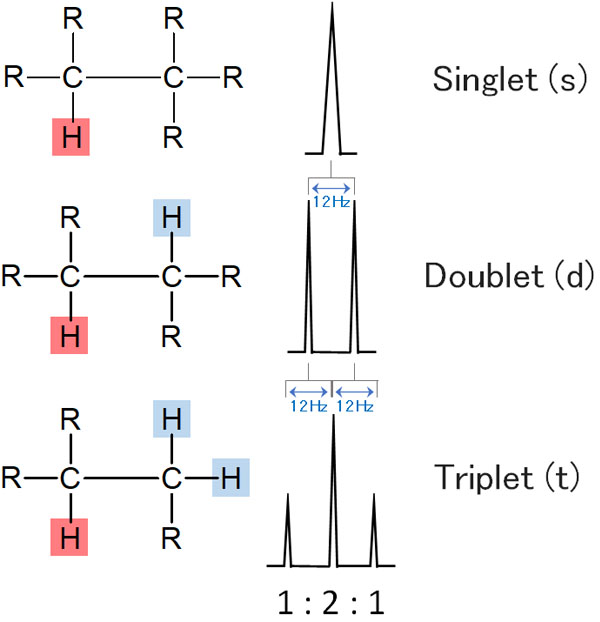
真ん中のピークが重なった結果、「1:2:1」の三重線となります。これをトリプレットといいます。
同じように考えると、「隣に水素原子が3つある状態」では四重線になります。これがカルテットです。また「隣に水素原子が4つある状態」では五重線になります。これをクインテットといいます。
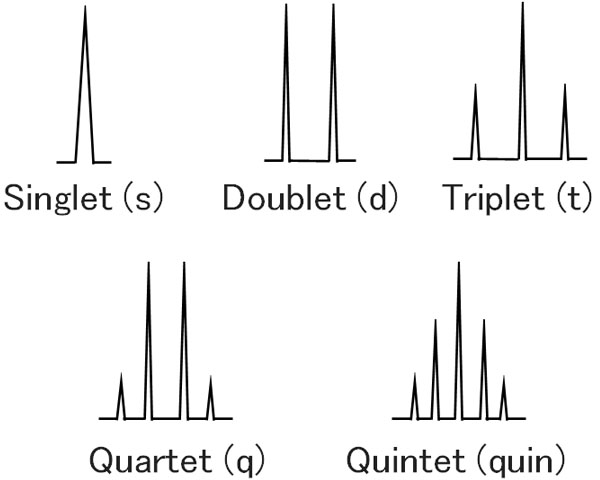
このようにして、NMRは隣にある水素の影響を受けてピークが分裂すると考えましょう。
・カップリングを生じる理由
なぜ、NMRでは隣にある水素の影響を受けるのでしょうか。これは、隣の水素のスピン状態が2つあるからです。具体的には、↑と↓の2つの状態を取れます。その結果、隣に水素が1つある場合、ダブレットになります。
一方で隣に水素が2つある場合はどうでしょうか。この場合、電子スピンの状態は以下の4種類が存在します。
- ↑ ↑
- ↑ ↓
- ↓ ↑
- ↓ ↓
ただ、↑ ↓と↓ ↑はエネルギーが同じです。つまり、同じものとみなすことができます。その結果、「1:2:1」の面積比のトリプレットとなります。これが、トリプレットやカルテット、クインテットを生じる理由です。
積分値(積分比)を見比べ、水素の数を推測する
さらには、NMRでは積分値(積分比)を調べなければいけません。積分値とは、NMRスペクトルが観測されたときの面積だと考えるようにしましょう。面積の度合いによって、炭素に結合したプロトンの数を推測できます。
例えば、以下のケースがあるとします。赤い水素原子に着目したとき、一つ目は水素がひとつだけです。ただ、二つ目は水素が二つです。
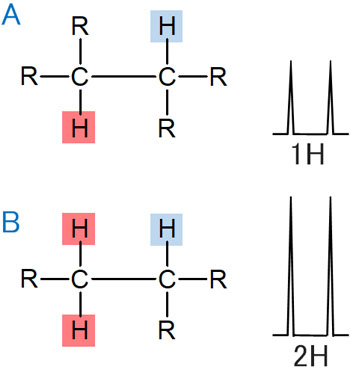
隣の炭素には水素原子が一つ結合しているため、ダブレットで観測されます。
ただAに比べて、Bは2倍の面積となります。この理由としては、Aは水素原子が1つだが、Bは水素原子が2つだからです。当然、その分だけ積分値は大きくなります。ここから、炭素に結合しているプロトンの数を容易に推測できます。
なお、実際には積分値として、水素ごとの面積比を算出します。NMRスペクトルからピークごとの積分値を出し、その面積比(積分比)を確認することで、構造決定できるようになるのです。
重DMSOまたは重クロロホルムとなる溶媒
それでは、実際にNMRを利用して測定するとき、どのようになるのでしょうか。これについて、測定したい化合物を溶媒に溶かさなければいけません。化合物が固体のままで測定できることはなく、液体だからこそ磁場をかけたときに2つのエネルギーに分けることができるのです。
つまり、溶かすための溶媒が必要です。溶かす溶媒は重DMSO(ジメチルスルホキシド)または重クロロホルムが一般的です。
DMSOはほとんどの化合物を溶かすことができます。そのため便利ですが、DMSOの値段は高いです。そのためNMR測定を何度も行う場合、DMSOを毎回利用していると、教授からは嫌な顔をされる可能性があります。
一方でクロロホルムは安いです。お金を失いたくない教授は、NMR測定のとき、積極的にクロロホルムの使用を推奨してくるでしょう。ただクロロホルムの場合、溶けにくい化合物がよくあります。その場合、仕方ないのでDMSOを利用するしかありません。
なお溶媒も化合物の一つであり、溶媒は水素をもっています。そのためあなたが測定したい化合物だけでなく、DMSOまたはクロロホルムのピークも観測されると理解しましょう。これを溶媒ピークといいます。NMRに表れる溶媒ピークは無視しましょう。
・重溶媒(重水素)だが溶媒ピークは存在する
ちなみに、利用される重DMSOや重クロロホルムの溶媒は重溶媒という特殊な液体になります。重溶媒とは、一般的な水素(1H)が重水素(2H)に置き換わったものになります。2Hのため、一般的な水素に比べて質量が重くなっています。
1H-NMRで測定するため、化合物を溶かす溶媒が1Hのままだと、溶媒のピークだけが観測されるようになります。測定したい化合物の量に比べて、溶媒量のほうが圧倒的に多いからです。そこで水素を重水素に置換することで、溶媒ピークができるだけ検出されないようにします。その結果、化合物のピークを検出できるようになります。
もちろん、完全に重水素へ置換できるわけではありません。そのため、溶媒ピークはどうしても表れると考えましょう。
TMS(テトラメチルシラン)がNMRの基準物質:化学シフトゼロ
またNMRで低磁場や高磁場を測定するとはいっても、基準となるポイントが分かりません。そこで、どこがゼロなのか明確に定める必要があります。何かと比較しなければ、正しい測定値かどうか分かりません。
そこでNMRでは、必ずTMS(テトラメチルシラン)という化合物を基準物質として入れます。一滴、測定する溶液に入れるだけです。
TMS(テトラメチルシラン)は以下のような構造をしています。
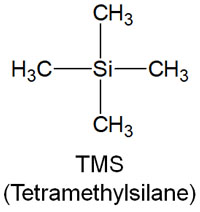
TMSはケイ素化合物であり、ケイ素原子の周りにはメチル基があります。その結果、非常に電子密度の高い化合物となっています。かなり高いエネルギーを与えなければピークが観測されないため、TMSが観測されるポイントをNMRではゼロと判断します。
TMSはかなりの高磁場にピークが表れるため、ここを基準(ゼロ)にします。これが、TMSが基準物質と呼ばれる理由です。TMSに比べて、どれくらい低磁場・高磁場にピークが表れるのかを観測するのがNMRです。
ピークが表れる位置を化学シフトといいます。TMSでは化学シフトがゼロと判断します。
NMRは単一化合物の構造式を確認するツール
なおNMR(核磁気共鳴)を利用する場合、大原則があります。それは、単一化合物だけを観測することです。2つ以上の化合物が混じった状態で測定してはいけません。
2つ以上の化合物が存在すると、NMRには複数化合物のピークが検出されるようになります。その結果、検出されたピークがどの化合物のものか判定できず、構造決定することができません。
もちろん、場合によっては溶液中に「メタノールが混じっていた」「酢酸が残っていた」などにより、これらの溶媒ピークが観測されることはあります。ただこの問題については、研究に慣れた人はすぐに判別できるため、大きな問題にはありません。
メタノールや酢酸のピークがどこに表れ、どのような形になるのかは容易に推測できます。
しかし、未知の化合物を測定するのがNMRです。そうしたとき、構造式が分からない未知の化合物が2つ以上混じっていると、構造決定は不可能だと理解しましょう。
分子量が大きく複雑すぎる構造、たんぱく質などの高分子は解析が困難
他にも、NMRで構造決定するときの注意点があります。それは、複雑すぎる構造の化合物は解析が難しくなることです。
水素原子の数や環境を測定する手法がNMRです。当然、構造が複雑でプロトン(水素原子)の数が多くなるほど、観測されるピークの数は多くなります。また、観測されるピークが重なってしまうケースも多くなります。その結果、分子量の大きい化合物は解析が困難になります。
これがたんぱく質などの高分子になると、構造決定は不可能です。分子量の大きい化合物でさえ構造決定が難しいです。ちなみに、たんぱく質は低くても分子量が4,000です。
1H-NMRは水素原子の環境を測定するツールです。そのため低分子化合物の測定に優れているツールであり、分子量の大きい化合物の構造決定には不向きです。これが、NMRを利用した構造決定の欠点です。
NMRの原理を学び、化学研究を行う
合成や抽出などによって単一の化合物を取り出したあと、次に行うべき操作が構造決定です。ターゲットとする化合物がどのような構造をしているのか、1H-NMRを利用することでプロトンの環境を調べ、構造決定するのです。
有機化学の研究室であれば、毎日のようにNMRを利用します。合成した化合物が目的物かどうか、調べる必要があるからです。
また未知の化合物を抽出する研究室でも、NMRを利用して構造決定をします。どのような構造式なのか、NMRの測定データから推測するのです。
化学研究の中では、NMRは使用頻度が高いです。そこでNMRの原理を学ぶ必要があります。ここではできるだけ簡単に分かりやすく解説したため、なぜNMRを利用するのかまで含めて学んでいきましょう。






