有機化合物の合成や分離をメインで行う研究室だと、毎日のように行う分析手法に薄層クロマトグラフィー(TLC)があります。
通常、クロマトグラフィーというと物質の分離を目的とします。もちろん、薄層クロマトグラフィーも化合物を分離できることには変わりません。
ただ、合成または抽出した大量の化合物を分けるのではなく、化合物の合成反応が完了したかどうかを確認するための手法が薄層クロマトグラフィー(TLC)です。または、溶液の中にいくつの化合物が混じっているのか確認するために使用されます。
原理について理解していないと、薄層クロマトグラフィーを利用することはできません。そこで原理や特徴、Rf値の読み方、展開溶媒の選び方まで含めて解説していきます。
もくじ
ガラス板にシリカゲル(固定相)を吸着させる
分析手法の中でも、ガラス板にシリカゲルを吸着させたものがTLCです。以下の薄い板がTLCであり、これを利用して化学実験での研究を行います。

薄層クロマトグラフィーではシリカゲルに限らず、アルミナを利用することがあります。ただアルミナではなく、シリカゲルが最も一般的です。特別な理由がない限り、アルミナではなく、シリカゲルのTLCを利用します。
薄層クロマトグラフィーは吸着クロマトグラフィーの一種です。吸着クロマトグラフィーでは、必ず固定相(動かない固体部分)が存在します。薄層クロマトグラフィーでは、シリカゲルが固定相になると理解しましょう。
またシリカゲルは以下の構造式となっています。
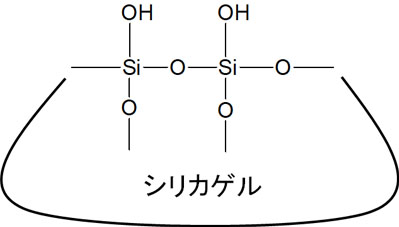
構造中に酸素原子が多く、シリカゲルは非常に極性の高い物質だといえます。この性質を利用して、化合物が正しく合成されているかどうかを確認します。
他のクロマトグラフィーとの違いは何か
そうしたとき、他のクロマトグラフィーとの違いは何でしょうか。クロマトグラフィーでは、他にも以下のようなものが存在します。
- カラムクロマトグラフィー
- HPLC(高速液体クロマトグラフィー)
- ペーパークロマトグラフィー
前述の通り、薄層クロマトグラフィーは物質を完全に分けるために行う実験操作ではありません。「有機合成反応が進んでいるか」「溶液中に化合物がいくつ存在するのか」などを確認する分析手法が薄層クロマトグラフィーです。
一方でカラムクロマトグラフィーやHPLC(高速液体クロマトグラフィー)は物質の分離が可能です。カラムクロマトグラフィーは化合物を完全に分離させるための手法になります。HPLCは化合物の分離だけでなく、検出や濃度測定なども可能です。
これらの分析手法に比べて、薄層クロマトグラフィーは「有機合成反応の進行度合い」「溶液中にいくつの化合物が存在するのか」のみ知ることができます。
またペーパークロマトグラフィーについては、シリカゲルの薄い板ではなく、固定相が紙になっています。そのため小学生の化学実験でも行える、非常に簡単な手法になります。大学研究でペーパークロマトグラフィーを行うことはないですが、子供たちの科学研究では活躍します。
極性の高い・低いでシリカゲル固定相の移動速度が異なる
それでは、なぜ固定相にシリカゲルを利用するのでしょうか。先に述べた通り、シリカゲルは非常に極性の高い物質だからです。
水は極性が高いです。一方、油(脂質)は極性が低いです。その結果、水と脂質が混じることはありません。
これと同様に考えてみましょう。シリカゲルは極性が高い固定相です。つまり、極性の高い化合物とは親和性が高いです。その結果、極性の高い化合物はシリカゲルと相互作用する(シリカゲルに吸着する)ようになります。
一方で脂溶性の高い化合物はシリカゲルと相互作用しにくいです。シリカゲルによる影響は少ないのです。
そうしたとき、2つ以上の化合物が存在する溶液をシリカゲル上で流します。そうすると、極性の低い化合物(脂溶性の高い化合物)はシリカゲルの影響が少なく、移動速度は速いです。一方、極性の高い化合物はシリカゲルに吸着されながら、少しずつ前に進みます。
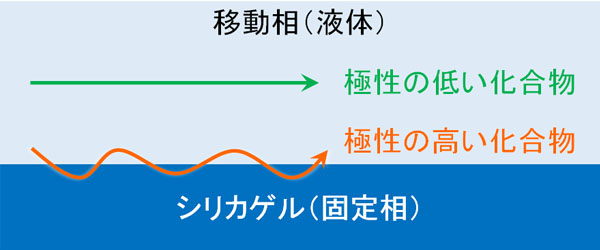
化合物によって極性の高い・低いは異なります。化合物の進むスピードの違いを利用して、溶液中の化合物がどのようになっているのか確認できるようになります。
移動相で利用する有機溶媒を考察する
次に薄層クロマトグラフィーで考えなければいけないのが移動相です。どのような有機溶媒を利用するのかを考察するのです。
薄層クロマトグラフィーは最初、TLCに溶液をスポットします。これを移動相(展開溶媒)に浸します。すると、溶媒が上昇してきます。溶媒の上昇に伴い、化合物も上へと移動します。ただ化合物によって移動速度が異なるため、化合物が分かれます。
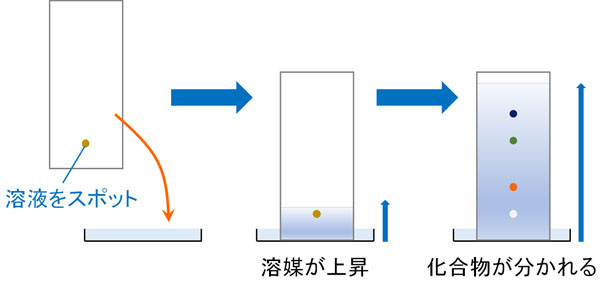
ただ、有機溶媒にはいくつもの種類があります。その中でも、最も一般的な展開溶媒が酢酸エチルとヘキサンです。一般的には、この2つの有機溶媒を混ぜ合わせ、TLCで用いる移動相(展開溶媒)を作成します。
酢酸エチルとヘキサンはそれぞれ、以下の構造式をしています。
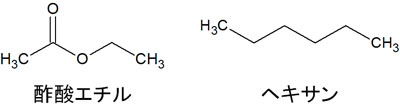
構造式を見て分かる通り、酢酸エチルは極性が高いです。そのため酢酸エチルの割合が大きいと、有機化合物はシリカゲルから酢酸エチルへ溶け出すようになります。つまり、移動相と一緒に前に進みやすくなります。
一方、ヘキサンは疎水性が非常に高く、ヘキサンに溶け出す化合物はほとんどありません。そのためヘキサンの割合が高い展開溶媒では、化合物が前に進むスピードは遅いです。
酢酸エチルとヘキサンを混ぜる割合について、1:1や1:3など多くの選択肢があります。ただ化合物によって性質が異なり、どの割合がいいのかは誰も分かりません。そこで、何度もTLCをして最適な割合を探し当てる必要があります。
Rf値は移動距離を表す
展開溶媒を決めて薄層クロマトグラフィーをしたとき、Rf値が決まります。Rf値とは、化合物が移動した距離を意味します。展開溶媒が移動した距離と化合物が移動した距離を算出することで、簡単にRf値を出せます。
- Rf値 = 化合物が移動した距離 ÷ 展開溶媒が移動した距離
例えば以下の状態では、Rf値はそれぞれ0.6と0.2です。
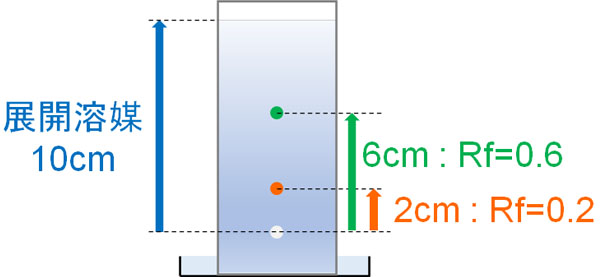
極性が高い化合物ほど、シリカゲルと相互作用します。シリカゲルに強く吸着されるため、前に進みにくく、Rf値は下がります。一方、疎水性の高い化合物はシリカゲルに吸着されにくいため、Rf値は高くなります。
もちろん、Rf値は展開溶媒によってまったく異なります。移動相で酢酸エチルの割合を高くすれば、化合物は極性の高い酢酸エチルと一緒に、素早く前に進んでいきます。
TLCは3点以上のスポットを打つ
なお、実際の実験でTLCを利用する場合、3点以上のスポットを打ちます。一つだけスポットを打つことはありません。
なぜ3点のスポットが必須なのでしょうか。これは、そうしなければ有機合成反応が進んでいるかどうか分からないからです。また、薄層クロマトグラフィーで観測されるスポットが原料かどうか判定する意味もあります。
科学実験では、基準となる物質を用意するのが原則です。薄層クロマトグラフィーでは、基準物質が原料です。例えば、以下の有機合成をする場面を考えてみましょう。
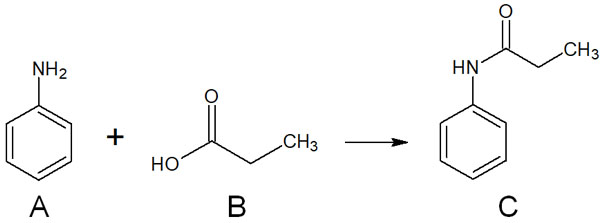
化合物を合成するとき、薄層クロマトグラフィーで化合物のスポットを検出するにしても、表れるスポットが原料Aなのか、それとも化合物Cなのか判断できません。基準となる物質がないため、反応が途中なのか、失敗しているのか、それともすべての合成反応が終わっているのかも不明です。
そこで、「原料A」「原料A+合成した溶液」「合成した溶液」の3点でスポットを打ちます。以下のようになります。
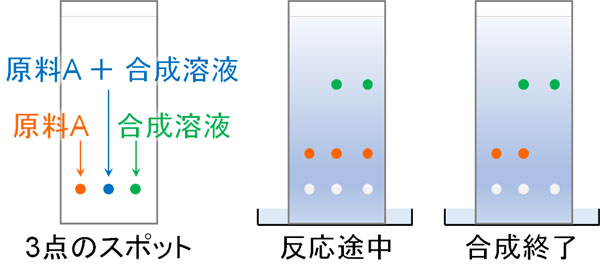
原料Aと同じ位置にスポットが観測される場合、そのスポットは原料Aと判断できます。また、一番右にスポットを打った合成溶液に原料Aが観測される場合、まだ溶液の中に原料Aが残っており、反応の途中だと判断できます。
一方で原料Aが消失すれば、合成終了です。TLCによって目的化合物を合成できたことを確認できます。
なお、原料Bをスポットしないのは理由があります。それは、容易には観測できないからです。薄層クロマトグラフィーでは主にUVランプを用いてスポットがあるかどうかを確認します。ただ原料BはUVランプで確認できないため、TLCにスポットを打ちません。
展開溶媒(移動相)を決める
なお、TLCに3点スポットを打ったあと、展開溶媒(移動相)を決めなければいけません。既に述べましたが、使用する有機溶媒は主に酢酸エチルとヘキサンを混ぜ合わせたものです。
酢酸エチルの割合が大きいと、Rf値は大きくなります。化合物は前に進みやすくなるのです。一方、ヘキサンの割合を大きくすると、Rf値は低くなります。酢酸エチルとヘキサンを混ぜる割合については、勘を頼りに実際に薄層クロマトグラフィーを何度も実施しながら、最適な展開溶媒を見つけましょう。
ただTLCの展開溶媒は酢酸エチルとヘキサンだけではありません。以下の組み合わせも存在します。
- ジクロロメタンとメタノール:極性が高い化合物に使う
- 酢酸エチルとメタノール:非常に極性が高い化合物に使う
- ヘキサンとジクロロメタン:非常に極性が低い化合物に使う
他にもありますが、基本はこれらの展開溶媒を利用します。
一般的には、酢酸エチルとヘキサンにてTLCの移動相を作成すれば問題ありません。ただ、この展開溶媒では無理なケースが稀にあります。その場合、他の有機溶媒を組み合わせることで展開溶媒を作成します。
紫外線照射(UVランプ)で共役のある化合物を判断する
ただ有機化合物のスポットを打つとはいっても、肉眼で有機化合物を見るのは不可能です。スポットを打ったとしても、有機溶媒が蒸発すれば、元の白い板になります。そうしたとき、どのようにして薄層クロマトグラフィーの有機化合物を確認すればいいのでしょうか。
これには、紫外線照射をします。UVランプを当てれば、有機化合物を確認できるようになるのです。
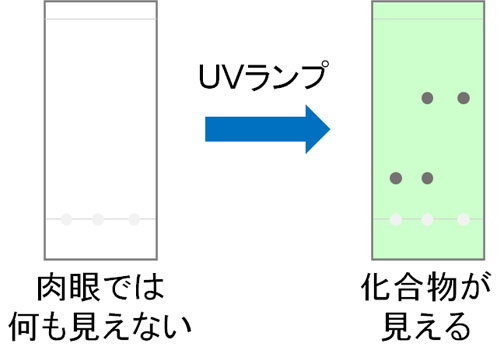
共役のある化合物は紫外線を吸収します。分かりやすい例であれば、構造式にベンゼン環を有する化合物はすべて紫外線を吸収し、蛍光を放つようになります。UVランプによって紫外線照射をすれば、ベンゼン環を含め、構造式に共役がある化合物はTLCで確認可能です。
先ほど、原料B(プロピオン酸)は薄層クロマトグラフィーでの観測が難しいと説明しました。これは、プロピオン酸に共役構造が存在せず、UVランプを利用してもTLCに蛍光が表れないからです。
・不純物があると、マルチスポットになる
なお実際の合成研究では、ターゲット化合物だけが生成されることは稀です。不純物として、その他の化合物も一緒に合成されてしまうことがよくあります。
紫外線照射すると、複数スポットが検出されるのは一般的です。その場合、スポットの色が薄い・濃いによって、ターゲット化合物や不純物がどれかを判断します。

または濃いスポットがいくつもある場合、それぞれの化合物をカラムクロマトグラフィーなどによって分離し、どれがターゲット化合物なのか調べる必要があります。
ニンヒドリン反応や焼くなど、その他の手法も可能
ただ、化合物のすべてが共役構造を有するとは限りません。ベンゼン環などの共役構造を有さない化合物はたくさん存在します。また、共役構造を持たない化合物同士で有機合成反応をすることもあります。その場合、紫外線照射をしても化合物を確認できません。
そうしたとき、その他の方法を試します。例えば、ニンヒドリン反応が知られています。アミノ酸を有する化合物であれば、TLCをニンヒドリンに浸すことで、色が変わるようになります。ニンヒドリン反応では、アミノ酸を有する化合物は紫色に変化します。
他には、TLCをオーブンで数分焼くという方法もあります。有機化合物のため、焼くと黒く焦げることがよくあるからです。化合物が熱によって蒸発する場合は無理ですが、そうでない場合は焼くことで化合物を見られるようになります。
薄層クロマトグラフィーの結果を確認するとき、化合物に色素がなかったり紫外線照射で蛍光がなかったりすることがあります。その場合、その他の方法によって結果を確認するようにしましょう。
有機化学の実験でTLCを利用する
分析手法の中でも、有機化学に関する研究をする場合、毎日のように利用するのが薄層クロマトグラフィーです。TLCを利用することで、合成反応が進んでいるかどうかを確認できます。また、溶液中に含まれる化合物の数も確認できます。
有機化合物を取り扱う場合は必須の分析手法のため、原理は必ず理解しましょう。固定相(吸着剤)としてシリカゲルを利用し、極性の高い化合物はシリカゲルに吸着されながら前に進みます。
利点は、非常に簡単な操作なので何度も行えることです。ただTLCは有機合成反応の進行度合いを確認するためのものです。また移動相を何にするのか、展開溶媒を考える必要があり、紫外線照射で確認できない有機化合物はたくさんあります。これが薄層クロマトグラフィーの欠点だといえます。
薄層クロマトグラフィーの原理を理解するためには、吸着材としてのシリカゲルの性質を学ばなければいけません。また移動相やRf値を理解するからこそ、合成研究で役立つようになります。理論は難しくないため、TLCの特徴や性質、利点・欠点を含めて把握しましょう。






