高校化学で有機化学の基礎を学ぶとき、アルデヒドとケトンの性質を理解する必要があります。酸素Oを含む化合物がアルデヒドとケトンです。
アルデヒドとケトンは性質が大きく異なります。ただ化学式は同じであり、構造異性体の関係になっています。アルデヒドとケトンは親せきの関係にあるため、有機化学を学ぶときはアルデヒドとケトンをセットで理解しましょう。
なおアルデヒドとケトンで重要な反応に銀鏡反応やフェーリング反応、ヨードホルム反応があります。アルデヒドやケトンが存在することを検出するとき、これらの反応が利用されます。
それでは、アルデヒドやケトンにはどのような性質があるのでしょうか。アルデヒドとケトンについて、合成法や性質、検出法を解説していきます。
もくじ
アルデヒド(ホルミル基)の性質:還元性と親水性
-CHOの構造をもつ化合物をアルデヒドといいます。官能基としては、-CHOはホルミル基と呼ばれます。主鎖に-CHOがある場合はアルデヒドになり、側鎖(官能基)として-CHOがある場合はホルミル基になるのです。
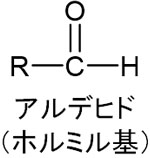
※高校化学の教科書では、ホルミル基をアルデヒド基と記していることがあります。ただ官能基でアルデヒド基はこの世に存在せず、明らかに間違っている記述です。そのためアルデヒド基ではなく、ホルミル基で覚えましょう。
アルデヒドには主に2つの性質があります。一つは還元性であり、還元剤として機能します。もう一つの特徴は親水性であり、水に溶けやすいです。アルデヒドには酸素Oが結合しているため極性が高くなり、水との親和性が高くなるのです。
ホルムアルデヒド、アセトアルデヒドの製法
それでは、ホルミル基を有する化合物の中で有名な化合物を覚えましょう。アルデヒドで有名な化合物はホルムアルデヒドとアセトアルデヒドです。それぞれの構造式は以下のようになります。

例えばホルマリンはホルムアルデヒドの水溶液であり、消毒剤や防腐剤としてホルマリンが利用されます。生物の個体や組織片をホルマリンに漬けることにより、標本作成するときに利用されるのです。
また、アセトアルデヒドはアルコールを飲んだあとの悪酔いの原因です。アルコールを飲んだあと、時間が経過すると体内のアセトアルデヒド濃度が上昇します。これにより、二日酔いになります。遺伝的にアセトアルデヒドの分解機能が弱い人はお酒に弱い体質です。
第一級アルコールを酸化すると、アルデヒドが生成されると知られています。そのためメタノールを酸化するとホルムアルデヒドとなり、エタノールを酸化するとアセトアルデヒドになります。
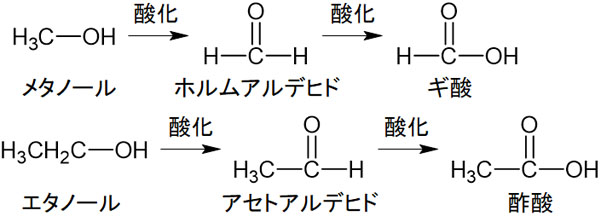
またアルデヒドを酸化すると、カルボン酸になることが知られています。そのためホルムアルデヒドを酸化するとギ酸になり、アセトアルデヒドを酸化すると酢酸になります。お酒に弱い人は遺伝的にアセトアルデヒドを酢酸へ変換する能力が弱いのです。
なおアルデヒドを合成するとき、アルキンにH2Oを付加させることによって合成することも可能です。例えばアセチレンにH2Oを付加反応させることによってビニルアルコールが生成されます。
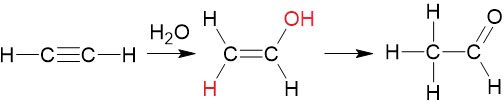
ただビニルアルコールは不安定な物質であるため、すぐに分解することによってアセトアルデヒドになります。
銀鏡反応・フェーリング反応によってアルデヒドを検出する
なお、アルデヒドの性質に還元性があることを先ほど解説しました。化合物にホルミル基が存在するかどうかを確かめる方法に銀鏡反応やフェーリング反応があります。これらの反応はアルデヒドによる還元性を用いた反応です。
・銀鏡反応(ぎんきょうはんのう)
銀イオンに過剰のアンモニアを加えると錯イオンを形成することが知られています。このとき、アンモニア性硝酸銀水溶液[Ag(NH3)2]+にアルデヒドを加えて加熱すると、銀Agの単体が析出します。この反応を銀鏡反応といいます。
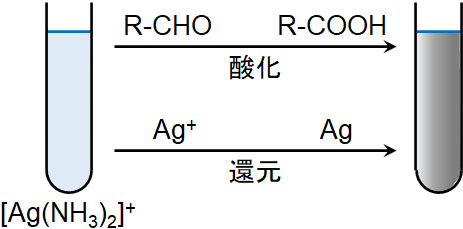
アルデヒドには還元作用があるため、自身は酸化されます。アルデヒドは酸化されることによってカルボン酸へと変化します。
一方、銀イオンは還元されて銀になります。銀の酸化数が+1から0へ変化することにより、還元反応が進行するのです。銀鏡反応では、試験管の側面に銀が付着します。
・フェーリング反応
ほかにも、ホルミル基が存在することを確認できる方法にフェーリング反応があります。フェーリング反応ではフェーリング液を利用します。フェーリング液には銅(Ⅱ)イオンCu2+が含まれています。
フェーリング液にアルデヒドを加えて加熱すると、アルデヒドによる還元作用によってCu2+は酸化銅(Ⅰ)Cu2Oへ変化します。そのため、銅の酸化数は+2から+1になります。
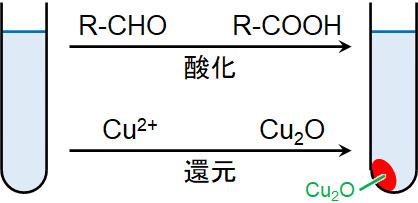
※Rはアルキル鎖を意味します。
Cu2+を含むため、フェーリング液は青色です。一方、Cu2Oは赤色の固体です。そのためCu2+が還元されてCu2Oになると、赤色沈殿を生じます。またアルデヒドは酸化されるため、カルボン酸になります。この反応がフェーリング反応です。
銀鏡反応またはフェーリング反応を起こす場合、化合物はホルミル基を含むと判断できます。
ケトン(カルボニル基)には還元性がなく、アルデヒドの構造異性体
アルデヒドと同じ化学式であり、構造異性体の関係にあるのがケトンです。そのためアルデヒドを学ぶとき、ケトンも同時に学びましょう。ケトンでは、官能基をカルボニル基といいます。以下がケトンの構造です。

-CO-の官能基がカルボニル基です。また化合物にR1-CO-R2の構造がある場合、その化合物をケトンといいます。酸素Oが存在するため、カルボニル基があると親水性が高まります。
※高校化学の教科書には、カルボニル基ではなくケトン基と記していることがあります。ただアルデヒド基と同様に、ケトン基は存在しません。そのため明らかに間違っている記述であり、必ずカルボニル基で覚えましょう。
アルデヒドとは異なり、ケトンには還元性がありません。そのためケトンは銀鏡反応やフェーリング反応を示しません。例えば、化学式C3H6Oをもつ化合物があるとします。この場合、化合物の候補としては以下の2つがあります。
- アセトアルデヒド:CH3CH2CHO
- アセトン:CH3COCH3
銀鏡反応またはフェーリング反応によって反応が進む場合、化合物はアセトアルデヒドです。一方で反応が進行しない場合、化合物はアセトンです。
アセトンの合成法:第二級アルコールの酸化やクメン法
それでは、どのようにしてケトンを合成すればいいのでしょうか。最も有名なケトンの合成法としては、第二級アルコールの酸化があります。アルコールを酸化する場合、第一級アルコール、第二級アルコール、第三級アルコールの違いによって以下のように生成物が異なります。
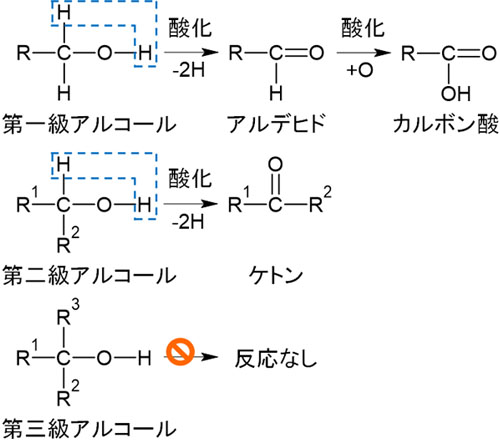
なおカルボニル基を含む化合物の中で最も有名な有機化合物がアセトンCH3COCH3です。そこで、アセトンの製法をより詳しく確認しましょう。
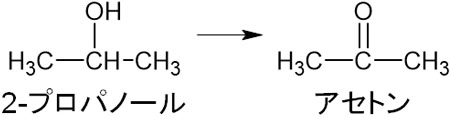
・2-プロパノールを酸化する
先ほど解説した通り、第二級アルコールを酸化することでケトンを得られます。アセトンを得たい場合、2-プロパノールを酸化しましょう。そうするとアセトンを得られます。
・酢酸カルシウムを乾溜する
酢酸カルシウム(CH3COO)2Caを乾溜することによってもアセトンを得ることができます。
- (CH3COO)2Ca → CH3COCH3 + CaCO3
空気を遮断して熱することで化合物を加水分解した後、揮発性物質と不揮発性物質に分ける操作を乾溜といいます。酢酸カルシウム(CH3COO)2Caを乾溜すると、アセトンCH3COCH3と炭酸カルシウムCaCO3を得ることができます。
・クメン法(工業的製法)での副生成物として得る
フェノールを得る工業的製法にクメン法があります。クメン法によってフェノールを合成する場合、副生成物としてアセトンを得ることができます。そのため、クメン法はアセトンの合成法でもあります。
高校化学でクメン法を学ぶ場合、製法を覚えましょう。反応機構は大学の有機化学で学ぶ難しい内容であるため、高校化学のような有機化学の基礎では反応機構を理解する必要はありません。
クメン法では、ベンゼンとプロペンを用いて付加反応させることでクメンを得ます。その後にO2を加え、希硫酸によって分解することでフェノールとアセトンを得ることができます。
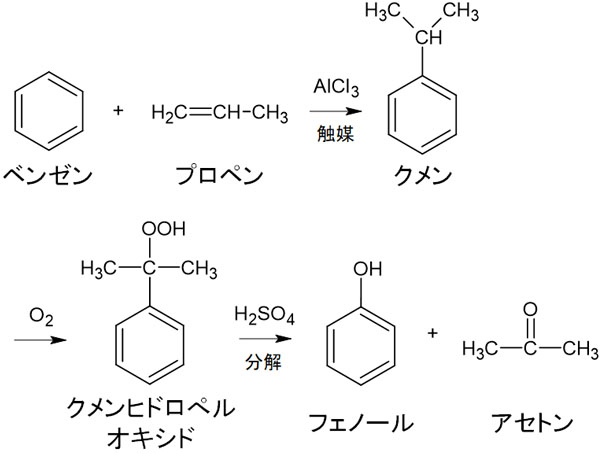
ひとまず、アセトンの製法としてクメン法があることを理解すれば問題ありません。
アセトンはヨードホルム反応を示す
それでは、アセトンが存在することを確認するためにはどのようにすればいいのでしょうか。前述の通り、ケトンには還元性がないので銀鏡反応やフェーリング反応は進行しません。
そこで、アセトンの検出ではヨードホルム反応を利用しましょう。以下の構造をもつアルデヒドやケトン、アルコールはヨードホルム反応を起こします。

ヨウ素と水酸化ナトリウム水溶液を加えると、ヨードホルムCHI3による黄色沈殿を生じる反応をヨードホルム反応といいます。ヨードホルム反応を示す場合、化合物は先に示した構造をもつとわかります。なお、ヨードホルムは特有のにおいをもつ黄色結晶です。
例えば有機化合物の化学式がC3H6Oとわかっているとします。この場合、化合物の候補としてアリルアルコール、アセトン、プロピオンアルデヒドの3つがあります。この中で先ほど示した構造をもつのはアセトンだけです。

ヨードホルム反応の反応式を覚える必要はありません。その代わり、特有のにおいをもつ黄色沈殿を生じた場合、ヨードホルム反応が起こったと推測できるようにしましょう。
なお、すべてのケトンがヨードホルム反応を示すわけではありません。ただ、アセトンはヨードホルム反応を示します。
・カルボン酸はヨードホルム反応を示さない
注意点として、カルボン酸はヨードホルム反応を示しません。そのため、酢酸はヨードホルム反応に関与しません。
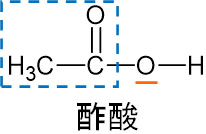
ヨードホルム反応を起こす構造では、RはHまたはアルキル鎖である必要があります。酢酸のようにRがOの場合、ヨードホルム反応を起こしません。
アルデヒドとケトンの特徴を学ぶ
重要な有機化合物がアルデヒドとケトンです。アルデヒドとケトンの両方とも親水性があります。官能基では、アルデヒドはホルミル基と呼び、ケトンではカルボニル基と呼ぶことは覚えましょう。
代表的なアルデヒドにはホルムアルデヒドとアセトアルデヒドがあります。両方とも有毒な化合物です。またアルデヒドには還元性があるため、銀鏡反応やフェーリング反応を起こします。それに対して、ケトンには還元性がありません。
また、ケトンで有名な有機化合物としてはアセトンがあります。アセトンには複数の製法があります。またヨードホルム反応を起こすのがアセトンの特徴であり、ヨードホルムは特有のにおいをもつ黄色の固体であることを覚えましょう。
ホルミル基とカルボニル基は重要な官能基であるため、有機化学の基礎を学ぶとき、どのような特徴があるのか理解しましょう。