非常に簡単な実験操作によって、化合物を還元できる手法に接触水素化があります。接触水素化は接触還元とも呼ばれています。
水素(H2)と反応させる手法が接触水素化です。接触還元によって水素が化合物に付加し、分子の形が変化します。
接触還元では、利用する試薬はほぼパラジウム炭素(Pd/C)になります。ただ、接触水素化には反応の種類がいくつもあります。どのような官能基について、どのような還元反応が起こるのか事前に学ばなければいけません。これにより、アルカンの合成や脱保護などが可能になります。
ここでは接触還元を用いた合成手法について、反応機構を含めて解説していきます。
もくじ
パラジウム炭素(Pd/C)を用いた接触水素化
還元剤を用いることで、化合物を還元することができます。ただ、こうした還元剤を利用するのではなく、水素と金属触媒を用いて合成反応を進めるのが接触水素化です。水素と付加反応させることで、分子の形を変化させます。
有機化学で頻繁に利用される金属触媒にパラジウムがあります。パラジウム炭素はパラジウム触媒の一つであり、活性炭にパラジウムを吸着させた物質がパラジウム炭素(Pd/C)です。
接触還元では、ほぼパラジウム炭素を用いて合成反応を進めることになります。場合によっては、アルキン(三重結合)からアルケン(二重結合)を合成したいときなど、リンドラー触媒という別のパラジウム触媒を利用しなければいけない場面があります。
ただ特別な理由がない限り、接触水素化による合成反応はパラジウム炭素を利用すると理解しましょう。
シン付加にて化合物を還元する反応機構
それでは、どのような反応機構によって接触還元が起こるのでしょうか。金属触媒(パラジウム炭素)を加え、水素を充満させた状態で化合物と反応させることで還元反応が進みます。
接触還元では、合成反応はパラジウム炭素の表面で起こります。最初、水素(H2)がパラジウム炭素の表面に吸着します。その後、化合物がパラジウム炭素に配位することで、分子に水素が付加されます。
例えば二重結合への接触水素化では、反応機構は以下になります。
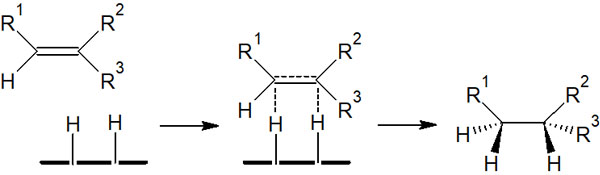
金属に吸着している水素原子と反応するため、同じ方向で水素付加されます。アンチ付加ではなく、シン付加にて合成反応が進みます。
接触還元で可能な合成反応の種類
それでは、接触還元ではどのような種類の合成反応があるのでしょうか。反応機構は単純であり、水素が付加されるだけです。ただ接触水素化によって可能な合成反応は種類が多く、それぞれの反応を学ばなければいけません。
接触水素化で重要な合成反応は以下の通りです。
- アルケン・アルキンをアルカンにする
- リンドラー触媒でアルケンを合成
- ベンジル基の脱保護
- ニトロ基・イミンの還元
- 芳香族ハロゲンの水素化
- アルデヒド・ケトンからのアルコール合成
接触水素化を行うとき、これらすべての反応を理解するのは必須です。二重結合を単結合にしたいと考えて合成反応をしたものの、例えば分子内にニトロ基が存在すると、ニトロ基はアミノ基へと変換されます。
接触還元は水素を反応させるため、立体障害は存在しません。また官能基に対する選択性もほぼありません。接触水素化で起こるあらゆる合成反応が進行するため、どのような還元反応が起こるのか理解する必要があります。
アルケン(二重結合)やアルキン(三重結合)をアルカンに変換する
接触水素化で還元するとき、代表的な方法がアルカンの合成です。分子内に二重結合や三重結合がある場合、接触還元によって単結合の化合物を合成できます。
前述の通り立体障害や官能基の選択性はなく、アルケンやアルキンが分子内にある場合、接触水素化によってすべての多重結合が単結合に変換されます。
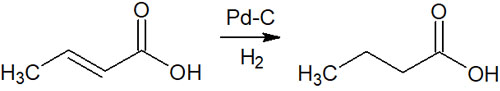
反応機構は難しくなく、先ほど述べた通りシン付加によって水素分子が付加します。その結果、アルケンやアルキンはアルカンに変換されます。
アルキン(三重結合)を接触還元するとき、パラジウム炭素(Pd-C)を利用してアルケン(二重結合)で合成を止めるのは無理です。分子内に存在する多重結合はすべてアルカン(単結合)に変換されます。
リンドラー触媒でアルキンからシス体(Z体)のアルケンを合成する
接触還元では、シン付加による位置選択性によって合成反応が進行します。そうしたとき、アルキンと反応させてアルケン(二重結合)を得ることはできないのでしょうか。
前述の通りパラジウム炭素を利用する場合、不可能です。その代わりリンドラー触媒を利用することで、アルキン(三重結合)からアルケン(二重結合)の合成が可能です。
リンドラー触媒でも、パラジウムを触媒として利用します。活性炭を含むのではなく、 炭酸カルシウム(CaCO3)にパラジウムを混ぜたものがリンドラー触媒です。なおリンドラー触媒では、酢酸鉛やキノリンを加えることで触媒の働きを低下させます。
物質を加えることで、触媒の作用を低下させることを触媒被毒といいます。酢酸鉛やキノリンは被毒作用があり、触媒能力の低下が可能なのです。
被毒によって触媒の働きが弱くなると、なぜ優れるのでしょうか。それはリンドラー触媒の働きが弱いことによって、アルケン(二重結合)からアルカン(単結合)へ合成させるときのスピードが非常に遅くなるからです。
そのためリンドラー触媒を利用すれば、シン付加によってアルキンからアルケンを合成できます。合成される化合物はすべてシス体(Z体)です。
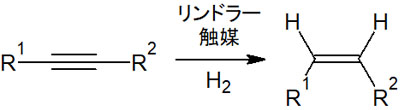
トランス化合物(E体)は生成されず、Z選択的にアルケンを得る方法の一つがリンドラー触媒の活用です。触媒の働きが強いとアルカンまで反応が進んでしまうものの、リンドラー触媒では二重結合をもつ化合物で合成反応が止まります。
ベンジル基の脱保護でパラジウム炭素を利用
脱保護をするときについても、接触還元は非常に重要な働きをします。アルコールの保護基として、ベンジル基が頻繁に利用されるからです。
アルコールは分極しており、反応性の高い官能基として知られています。そこで副反応を起こさないように、アルコールをベンジル基で保護します。ベンジルエーテルにしておけば、ヒドロキシ基(-OH)による反応性はなくなり、副反応が起こらなくなります。
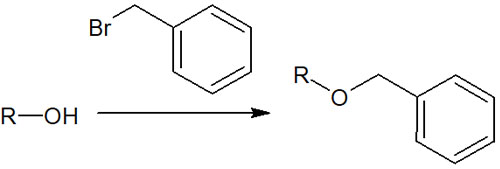
ベンジル基を保護基として利用する場合、脱保護の方法が接触還元です。水素とパラジウム炭素(Pd/C)を混ぜ、反応させることでベンジル基が外れます。
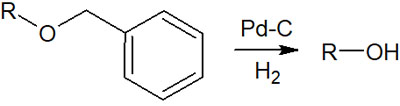
ベンジル基は酸性や塩基性など、さまざまな条件で保護基が取れにくいという利点があります。接触還元でなければ、ベンジル基の脱保護は難しいです。一方で脱保護の選択肢が接触水素化くらいしかなく、脱保護の選択肢が少ないのは欠点でもあります。
ニトロ基やイミンを還元し、アミンを得る
官能基の還元では、ニトロ基やイミンでも接触還元が利用されます。特にニトロ基を還元し、アミンを得る方法として接触水素化は頻繁に利用されます。
ニトロ基やイミンの還元方法としてはいくつか存在します。それらの中でも、接触水素化は非常に簡便な方法の一つです。水素ガスを充満させ、パラジウム炭素を加えて撹拌するだけだからです。また、反応終了後の後処理も簡単です。
接触還元により、以下のようにニトロ基はアミノ基になります。
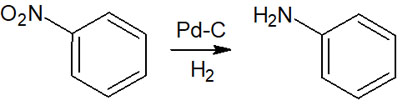
ニトロ基やイミンを還元するとき、有用性の高い合成反応が接触水素化です。
ベンゼン環の脱ハロゲン化
ベンゼン環に結合しているハロゲンについても、接触還元によって還元されます。ハロゲンの中でも、フッ素原子(F)はパラジウム炭素を用いて合成しても変化はありません。ただ塩素原子(Cl)や臭素原子(Br)、ヨウ素原子(I)については、脱ハロゲン化します。
例えばクロロベンゼンに対して接触還元をすると、以下のようにベンゼンが合成されます。
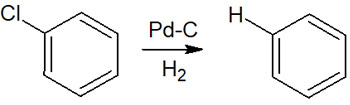
いずれにしても、ベンゼン環に結合しているClやBr、Iについては、接触還元によって水素原子に置換されると理解しましょう。
・塩化スズ(SnCl2)はベンゼン環上のハロゲンを還元しない
それでは、ベンゼン環上のハロゲンへの影響なしに還元するにはどうすればいいのでしょうか。この場合、接触還元とは異なる方法によって合成を進めます。
例えば、分子を還元できる試薬として塩化スズ(SnCl2)が知られています。塩化スズを利用すれば、ベンゼン環上のハロゲンが還元されず、他の部分を還元できます。例えば以下のように、ハロゲンの水素置換なしに、ニトロ基を還元してアミノ基を合成できます。
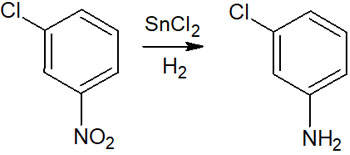
接触還元は簡便な手法なので頻繁に用いられますが、化合物によって還元方法を使い分けなければいけません。
アルデヒドやケトンをアルコールまたはメチレンへ還元する
またアルデヒド(ホルミル基)やケトン(カルボニル基)を有する化合物について、接触水素化によって還元することができます。還元することによって、アルコールまたはメチレンの化合物が得られます。
生成化合物がアルコールになるのか、またはメチレンになるのかについては、利用するパラジウム炭素の種類や反応条件によって異なります。
パラジウム炭素(Pd/C)には種類があります。そのため、どのパラジウム炭素を利用するのかによって、アルコールを得られるのか、またはメチレンへ還元されるのかが変わるのです。
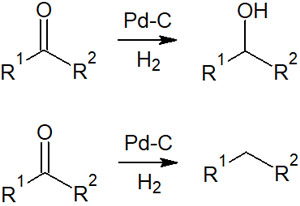
それぞれの違いについては、かなりニッチな内容になるので説明を省きます。重要なのは、アルデヒドやケトンを接触還元によって還元できる事実です。どのようなパラジウム炭素を利用することで、生成物がアルコールまたはメチレンになるのかについては、実験前に論文を読んで自ら調べましょう。
・エステルやカルボン酸は還元されない
なお、カルボニル化合物の中で還元される官能基はアルデヒドとケトンです。エステルやカルボン酸については、接触還元によって還元されません。
C=Oの構造があれば、必ずしもアルコールやメチレンに還元されるわけではありません。エステルとカルボン酸は接触水素化による還元の影響を受けないことを理解しましょう。
なお、エステルやカルボン酸の場合はヒドリド還元剤が還元反応で利用されます。ヒドリド還元剤は接触水素化とは異なる反応であり、合成したい化合物によって還元反応を使い分けましょう。
接触水素化で起こる反応を把握する
頻繁に利用される有機合成反応の一つが接触水素化です。アルカンを合成したり、脱保護をしたりなどと、多くの場面で利用されます。主にパラジウム炭素が利用されますが、アルキンからアルケンを合成するときはリンドラー触媒を利用します。
ここまで述べた接触還元の種類については、すべて覚える必要があります。特定の反応だけ制御することが難しいからです。
例えば分子内にベンジル基とニトロ基がある場合、接触還元によって両方の置換基が還元されます。一方だけを還元するためには、別の合成方法を検討しなければいけません。接触水素化で可能な還元反応を覚えているからこそ、最適な合成方法を選択できるようになります。
あらゆる有機化学の研究室で利用される合成方法の一つが接触還元です。接触水素化を利用し、目的化合物を得るようにしましょう。






